Etravirin
| |
|---|---|
| |
| Nama sistematis (IUPAC) | |
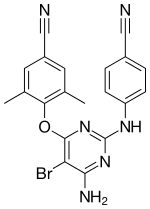
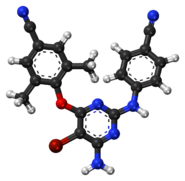
| 4-[6-Amino-5-bromo-2-[(4-sianofenil)amino] pirimidin-4-il]oksi-3,5-dimetilbenzonitril | |
| Data klinis | |
| Nama dagang | Intelence |
| AHFS/Drugs.com | monograph |
| MedlinePlus | a608016 |
| Data lisensi | US Daily Med:pranala |
| Kat. kehamilan | B1(AU) |
| Status hukum | Harus dengan resep dokter (S4) (AU) Schedule VI (CA) POM (UK) ℞-only (US) |
| Rute | oral |
| Data farmakokinetik | |
| Ikatan protein | 99.9% |
| Metabolisme | Hati (dimediasi CYP3A4, CYP2C9, & CYP2C19) |
| Waktu paruh | 41±20 jam |
| Ekskresi | Feses (93,7%), urin (1,2%) |
| Pengenal | |
| Nomor CAS | 269055-15-4 |
| Kode ATC | J05AG04 |
| PubChem | CID 193962 |
| DrugBank | DB06414 |
| ChemSpider | 168313 |
| UNII | 0C50HW4FO1 |
| KEGG | D04112 |
| ChEMBL | CHEMBL308954 |
| NIAID ChemDB | AIDSNO:105156 |
| Sinonim | TMC125 |
| Data kimia | |
| Rumus | C20H15BrN6O |
| |
Etravirin (disingkat ETR,[1]) adalah obat antiretroviral yang digunakan untuk penanganan HIV/AIDS. Etravirin adalah penghambat transkriptase balik non-nukleosida (NNRTI) HIV tipe 1.[2] Tidak seperti agen dalam kelas tersebut, resistensi terhadap NNRTI lain tampaknya tidak menyebabkan resistensi terhadap etravirin.[3] Etravirin dipasarkan oleh Janssen Pharmaceuticals, anak perusahaan dari Johnson & Johnson. Pada bulan Januari 2008, Badan Pengawas Obat dan Makanan Amerika Serikat (FDA) menyetujui penggunaannya untuk orang-orang dengan resistensi yang sudah ada terhadap obat lain, menjadikannya obat anti-HIV ke-30 yang disetujui di Amerika Serikat dan yang pertama disetujui pada tahun 2008.[4] Obat ini juga disetujui untuk digunakan di Kanada pada bulan April 2008.[5]
Etravirin dilisensikan di Amerika Serikat, Kanada, Israel, Rusia, Australia, Selandia Baru, dan Uni Eropa,[6] dan sedang dalam tinjauan regulasi di Swiss.[7]
Kegunaan dalam medis
[sunting | sunting sumber]Di AS, etravirin diindikasikan untuk pengobatan infeksi HIV-1 pada pasien yang sudah pernah menjalani pengobatan berusia dua tahun ke atas.[2]
Di Uni Eropa, etravirin dikombinasikan dengan penghambat protease yang ditingkatkan dan antiretroviral lainnya, diindikasikan untuk pengobatan infeksi HIV tipe 1 pada orang yang sudah pernah menjalani pengobatan antiretroviral berusia enam tahun ke atas.[8]
Kontraindikasi
[sunting | sunting sumber]Orang dengan masalah keturunan langka berupa intoleransi galaktosa, defisiensi Lapp laktase atau malabsorpsi glukosa-galaktosa tidak boleh mengonsumsi obat ini.[9]
Efek samping
[sunting | sunting sumber]Pada tahun 2009, informasi resep FDA untuk etravirin dimodifikasi untuk mencakup "laporan pasca pemasaran kasus sindrom Stevens-Johnson, nekrolisis epidermal toksik, dan eritema multiform, serta reaksi hipersensitivitas yang ditandai dengan ruam, temuan konstitusional, dan terkadang disfungsi organ termasuk gagal hati."[10]
Mekanisme kerja
[sunting | sunting sumber]Etravirin adalah NNRTI generasi kedua, yang dirancang untuk aktif melawan HIV dengan mutasi yang memberikan resistensi terhadap dua NNRTI generasi pertama yang paling sering diresepkan, mutasi K103N untuk efavirenz dan Y181C untuk nevirapin.[11] Potensi ini tampaknya terkait dengan fleksibilitas etravirin sebagai sebuah molekul. Etravirin adalah suatu diarilpirimidina (DAPY), sejenis molekul organik dengan beberapa isomerisme konformasi yang dapat mengikat enzim transkriptase balik dalam beberapa konformasi, memungkinkan interaksi yang lebih kuat antara etravirin dan enzim, bahkan dengan adanya mutasi.[12]
Kimia
[sunting | sunting sumber]Etravin terbentuk sebagai kristal ortorombik tak berwarna dalam grup ruang Pna21.[13] Struktur kristal ini dan sejumlah bentuk solvat dan garam telah dilaporkan.[13][14]
Penelitian
[sunting | sunting sumber]Etravin telah dipelajari untuk digunakan dalam aplikasi reposisi obat. Etravirin terbukti menyebabkan peningkatan produksi frataksin.[15]
Referensi
[sunting | sunting sumber]- ^ "Appendix A: Key to Acronyms". Guidelines for the Use of Antiretroviral Agents in HIV-1-Infected Adults and Adolescents. Department of Health and Human Services. Diarsipkan dari versi asli tanggal 31 August 2012.
- ^ a b "Intelence- etravirine tablet". DailyMed. 15 August 2023. Diakses tanggal 14 August 2024.
- ^ Stellbrink HJ (October 2007). "Antiviral drugs in the treatment of AIDS: what is in the pipeline ?". European Journal of Medical Research. 12 (9): 483–495. PMID 17933730.
- ^ "FDA Approves HIV Drug Etravirine". Associated Press. 18 January 2008.[pranala nonaktif]
- ^ "First New NNRTI in Nearly a Decade to Benefit Canadians with HIV/AIDS" (PDF) (Siaran pers). Janssen-Ortho Inc. 1 April 2008. Diarsipkan dari versi asli (PDF) tanggal 2 November 2010. Diakses tanggal 9 July 2008.
- ^ "Intelence receives marketing authorisation in the European Union for HIV combination therapy". Tibotec. Diarsipkan dari versi asli tanggal 28 September 2011. Diakses tanggal 29 August 2008.
- ^ "Etravirine (TMC125, Intelence) granted accelerated approval in US". aidsmap. Diarsipkan dari versi asli tanggal 2 January 2010. Diakses tanggal 24 January 2008.
- ^ "Intelence EPAR". European Medicines Agency (EMA). 28 August 2008. Diakses tanggal 14 August 2024. Text was copied from this source which is copyright European Medicines Agency. Reproduction is authorized provided the source is acknowledged.
- ^ "Etravine: Summary of product characteristics" (PDF). EMEA. hlm. 5. Diarsipkan dari versi asli (PDF) tanggal 20 August 2016. Diakses tanggal 13 July 2011.
- ^ "FDA Medwatch Safety Information". Food and Drug Administration. Diakses tanggal 27 August 2009.[pranala nonaktif]
- ^ Evans D (15 January 2008). "Etravirine—Countdown to Launch". AIDSmeds.com. Diarsipkan dari versi asli tanggal 19 January 2008. Diakses tanggal 2 February 2008.
- ^ Das K, Clark AD, Lewi PJ, Heeres J, De Jonge MR, Koymans LM, Vinkers HM, Daeyaert F, Ludovici DW, Kukla MJ, De Corte B, Kavash RW, Ho CY, Ye H, Lichtenstein MA, Andries K, Pauwels R, De Béthune MP, Boyer PL, Clark P, Hughes SH, Janssen PA, Arnold E (May 2004). "Roles of conformational and positional adaptability in structure-based design of TMC125-R165335 (etravirine) and related non-nucleoside reverse transcriptase inhibitors that are highly potent and effective against wild-type and drug-resistant HIV-1 variants". Journal of Medicinal Chemistry. 47 (10): 2550–2560. doi:10.1021/jm030558s. PMID 15115397.
- ^ a b Rajput L, Sanphui P, Desiraju GR (7 August 2013). "New Solid Forms of the Anti-HIV Drug Etravirine: Salts, Cocrystals, and Solubility". Crystal Growth & Design. 13 (8): 3681–3690. doi:10.1021/cg4007058. ISSN 1528-7483.
- ^ Muresan-Pop M, Macavei S, Turza A, Borodi G (November 2021). "New solvates and a salt of the anti-HIV compound etravirine". Acta Crystallographica Section C: Structural Chemistry. 77 (Pt 11): 698–706. doi:10.1107/S2053229621010482. PMID 34738540 Periksa nilai
|pmid=(bantuan). - ^ Alfedi G, Luffarelli R, Condò I, Pedini G, Mannucci L, Massaro DS, Benini M, Toschi N, Alaimo G, Panarello L, Pacini L, Fortuni S, Serio D, Malisan F, Testi R, Rufini A (March 2019). "Drug repositioning screening identifies etravirine as a potential therapeutic for friedreich's ataxia". Movement Disorders. 34 (3): 323–334. doi:10.1002/mds.27604. PMID 30624801.
