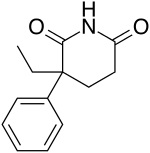
Glutetimid
| |
|---|---|
| |
| Nama sistematis (IUPAC) | |
| 3-etil-3-fenil-piperidina-2,6-diona | |
| Data klinis | |
| Nama dagang | Doriden, Elrodorm, Noxyron, dll |
| Kat. kehamilan | C: (Amerika Serikat) |
| Status hukum | Dikontrol (S8) (AU) Schedule IV (CA) ? (UK) Schedule II (US) |
| Kemungkinan ketergantungan |
Sedang hingga berat |
| Rute | Oral |
| Data farmakokinetik | |
| Bioavailabilitas | Bervariasi (Tmax = 1–6 jam)[1] |
| Ikatan protein | ~50% |
| Metabolisme | Secara luas di hati |
| Waktu paruh | 8–12 jam |
| Ekskresi | Ginjal |
| Pengenal | |
| Nomor CAS | 77-21-4 |
| Kode ATC | N05CE01 |
| PubChem | CID 3487 |
| Ligan IUPHAR | 7192 |
| DrugBank | DB01437 |
| ChemSpider | 3367 |
| UNII | C8I4BVN78E |
| KEGG | D00532 |
| ChEMBL | CHEMBL1102 |
| Data kimia | |
| Rumus | C13H15NO2 |
| |
| Data fisik | |
| Titik lebur | 84 °C (183 °F) |
| Kelarutan dalam air | 999 mg/L (30 °C/86 °F) mg/mL (20 °C) |
Glutetimid adalah obat sedatif-hipnotik yang diperkenalkan oleh Ciba[2] pada tahun 1954 sebagai alternatif yang aman untuk barbiturat untuk mengobati insomnia. Namun tak lama kemudian, menjadi jelas bahwa glutetimid juga dapat menyebabkan kecanduan dan menyebabkan gejala putus obat yang serupa. Tingkat produksi saat ini di Amerika Serikat (kuota tahunan untuk produksi yang ditetapkan oleh DEA adalah tiga gram, cukup untuk enam tablet glutetimid selama beberapa tahun) menunjukkan bahwa obat ini hanya digunakan dalam penelitian skala kecil. Produksi obat ini dihentikan di AS pada tahun 1993 dan dihentikan di beberapa negara Eropa Timur pada tahun 2006.

Penggunaan jangka panjang
[sunting | sunting sumber]Efek samping penggunaan jangka panjang, yang mirip dengan efek samping yang terlihat pada penghentian penggunaan barbiturat, secara anekdot telah dijelaskan pada pasien yang masih mengonsumsi dosis obat yang stabil. Gejalanya meliputi delirium, halusinosis, kejang, dan demam.[3]
Penggunaan rekreasi
[sunting | sunting sumber]Glutetimid adalah penginduksi enzim CYP2D6. Bila dikonsumsi dengan kodein (dikenal di jalanan sebagai "hits", "cibas and codeine", "Dors and 4s"), obat ini memungkinkan tubuh mengubah kodein dalam jumlah yang lebih banyak menjadi morfin. Efek sedatif umum glutetimid juga menambah efek kombinasi tersebut.[4] Sejumlah kematian telah terjadi akibat penyalahgunaan kombinasi ini.[5] Efeknya juga digunakan secara klinis, termasuk beberapa penelitian pada tahun 1970-an di berbagai negara tentang penggunaannya dalam keadaan yang dipantau secara ketat sebagai bentuk terapi substitusi agonis opioid oral, misalnya sebagai Substitutionmittel yang mungkin merupakan alternatif yang berguna untuk metadon.[6][7] Permintaan untuk kombinasi ini di Philadelphia, Pittsburgh, Newark, NYC, Boston, Baltimore, dan daerah sekitarnya di negara bagian Amerika Serikat lain dan mungkin di tempat lain, telah menyebabkan sintesis klandestin skala kecil glutetimid sejak 1984,[8] sebuah proses yang, seperti sintesis metakualon, agak sulit dan penuh dengan potensi hasil buruk ketika ahli kimia amatir memproduksi obat-obatan dengan prekursor tingkat industri tanpa kontrol kualitas yang memadai. Fakta bahwa sintesis klandestin yang lebih sederhana dari depresan farmasi punah lainnya seperti ethklorvinol, metiprilon, atau barbiturat tertua tidak dilaporkan tampaknya menunjukkan tingkat motivasi yang tinggi di sekitar obat yang unik, sekali lagi seperti metakualon. Produksi glutetimid dihentikan di AS pada tahun 1993 dan di beberapa negara Eropa Timur, terutama Hungaria, pada tahun 2006. Analisis glutetimid yang disita tampaknya selalu menunjukkan obat atau hasil sintesis yang dicoba, sedangkan metakualon yang diduga dalam sebagian besar kasus ditemukan inert, atau mengandung difenhidramin atau benzodiazepin.[8]
Status hukum
[sunting | sunting sumber]Glutetimid adalah obat Jadwal II di bawah Konvensi Psikotropika.[9] Awalnya ini adalah obat Jadwal III di Amerika Serikat di bawah Controlled Substances Act, tetapi pada tahun 1991 ditingkatkan ke Jadwal II,[10] beberapa tahun setelah ditemukan bahwa penyalahgunaan dikombinasikan dengan kodein meningkatkan efek kodein, dan kematian telah terjadi akibat kombinasi tersebut.[11][12] Ia memiliki DEA ACSCN sebesar 2550 dan kuota produksi tahun 2013 sebesar 3 g.
Sintesis
[sunting | sunting sumber]Isomer (R) memiliki onset yang lebih cepat dan aktivitas antikonvulsan yang lebih kuat pada model hewan daripada isomer (S).[13]

Penambahan konjugat yang dikatalisis basa dari 2-fenilbutironitril [769-68-6] (1) ke etil akrilat (2) menghasilkan etil 4-siano-4-fenilheksanoat, CID:139890735 (3). Hidrolisis basa dari gugus nitril menjadi gugus amida, dan siklisasi asam selanjutnya dari produk tersebut menghasilkan glutetimid yang diinginkan (4).
Referensi
[sunting | sunting sumber]- ^ Barceloux, Donald G. (2012). Medical Toxicology of Drug Abuse: Synthesized Chemicals and Psychoactive Plants. Hoboken, N.J.: John Wiley & Sons, Inc. hlm. 492–493. ISBN 978-0-471-72760-6. OCLC 814224300.
- ^ a b US patent 2673205, Hoffmann K, Tagmann E, "3-Disubstituted Dioxopiperidines and the Manufacture thereof", dikeluarkan tanggal 23 March 1954, diberikan kepada CIBA
- ^ Cookson JC (September 1995). "Rebound exacerbation of anxiety during prolonged tranquilizer ingestion". Journal of the Royal Society of Medicine. 88 (9): 544. PMC 1295346
 . PMID 7562864.
. PMID 7562864.
- ^ Shamoian CA (1975). "Codeine and glutethimide. Euphoretic, addicting combination". New York State Journal of Medicine. 75 (1): 97–99. PMID 1053824.
- ^ Havier RG, Lin R (April 1985). "Deaths as a result of a combination of codeine and glutethimide". Journal of Forensic Sciences. 30 (2): 563–6. doi:10.1520/JFS11840J. PMID 3998703.
- ^ Popa D, Loghin F, Imre S, Curea E (August 2003). "The study of codeine-gluthetimide pharmacokinetic interaction in rats". Journal of Pharmaceutical and Biomedical Analysis. 32 (4–5): 867–77. doi:10.1016/s0731-7085(03)00189-4. PMID 12899973.
- ^ Khajawall AM, Sramek JJ, Simpson GM (August 1982). "'Loads' alert". The Western Journal of Medicine. 137 (2): 166–8. PMC 1274052
 . PMID 7135952.
. PMID 7135952.
- ^ a b Gahlinger, Paul (2003). "Methaqualone and Glutethimide". Illegal Drugs: A Complete Guide to Their History, Chemistry, Use, and Abuse. ISBN 9780452285057. OCLC 52269170.
- ^ "List of psychotropic substances under international control" (PDF). International Narcotics Control Board. Diarsipkan dari versi asli (PDF) tanggal 2012-08-31.
- ^ "Section 1308.12 Schedules of Controlled Substances". Title 21 Code of Federal Regulations. Drug Enforcement Administration. Diarsipkan dari versi asli tanggal 2015-08-04. Diakses tanggal 2011-10-07.
- ^ Havier RG, Lin R (April 1985). "Deaths as a result of a combination of codeine and glutethimide". Journal of Forensic Sciences. 30 (2): 563–6. doi:10.1520/JFS11840J. PMID 3998703.
- ^ Feuer E, French J (February 1984). "Descriptive epidemiology of mortality in New Jersey due to combinations of codeine and glutethimide". American Journal of Epidemiology. 119 (2): 202–7. doi:10.1093/oxfordjournals.aje.a113738. PMID 6695899.
- ^ Houlihan WJ, Bennett GB (January 1977). "Anti-Anxiety Agents, Anticonvulsants and Sedative-Hypnotics". Annual Reports in Medicinal Chemistry. Academic Press. 12: 10–19. doi:10.1016/S0065-7743(08)61540-7.
- ^ Tagmann E, Sury E, Hoffmann K (1952). "Über Alkylenimin-Derivate. 2. Mitteilung". Helvetica Chimica Acta. 35 (5): 1541–1548. doi:10.1002/hlca.19520350516.
- ^ Salmon-Legagneur F, Neveu C (January 1952). "Sur Les Acides Alpha-Phenyl Alpha-Alcoyl (Ou Phenoalcoyl) Glutariques". Comptes Rendus Hebdomadaires des Séances de l'Académie des Sciences. 234 (10): 1060–2.
- ^ Salmon-Legagneur F, Neveu C (1953). "Sur Les Acides Alpha-Phenyl Alpha-Alcoyl (Ou Phenoalcoyl) Glutariques". Bull. Soc. Chim. France: 70.
- ^ DE patent 950193, Hoffmann K Tagmann E, "Verfahren zur Herstellung neuer Dioxopiperidine", dikeluarkan tanggal 4 October 1956, diberikan kepada CIBA
