Selenium
34Se Selenium | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 Selenium amorf hitam dan merah | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
Garis spektrum selenium | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sifat umum | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Pengucapan | /sèlènium/[1] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Penampilan | alotrop abu-abu tampak metalik, merah, dan hitam seperti kaca (tidak difoto) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Selenium dalam tabel periodik | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nomor atom (Z) | 34 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Golongan | golongan 16 (kalkogen) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Periode | periode 4 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Blok | blok-p | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kategori unsur | nonlogam poliatomik, kadang-kadang dianggap metaloid | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Berat atom standar (Ar) |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Konfigurasi elektron | [Ar] 3d10 4s2 4p4 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektron per kelopak | 2, 8, 18, 6 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sifat fisik | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fase pada STS (0 °C dan 101,325 kPa) | padat | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Titik lebur | 494 K (221 °C, 430 °F) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Titik didih | 958 K (685 °C, 1265 °F) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kepadatan mendekati s.k. | abu-abu: 4,81 g/cm3 alfa: 4,39 g/cm3 seperti kaca: 4,28 g/cm3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| saat cair, pada t.l. | 3,99 g/cm3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Titik kritis | 1766 K, 27,2 MPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kalor peleburan | abu-abu: 6,69 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kalor penguapan | 95,48 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kapasitas kalor molar | 25,363 J/(mol·K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
Tekanan uap
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sifat atom | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Bilangan oksidasi | −2, −1, 0,[2] +1,[3] +2, +3, +4, +5, +6 (oksida asam kuat) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronegativitas | Skala Pauling: 2,55 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Energi ionisasi | ke-1: 941,0 kJ/mol ke-2: 2045 kJ/mol ke-3: 2973,7 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Jari-jari atom | empiris: 120 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Jari-jari kovalen | 120±4 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Jari-jari van der Waals | 190 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Lain-lain | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kelimpahan alami | primordial | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Struktur kristal | trigon | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kecepatan suara batang ringan | 3350 m/s (suhu 20 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ekspansi kalor | amorf: 37 µm/(m·K) (suhu 25 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Konduktivitas termal | amorf: 0,519 W/(m·K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Arah magnet | diamagnetik[4] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Suseptibilitas magnetik molar | −25,0×10−6 cm3/mol (298 K)[5] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Modulus Young | 10 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Modulus Shear | 3,7 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Modulus curah | 8,3 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Rasio Poisson | 0,33 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Skala Mohs | 2,0 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Skala Brinell | 736 MPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nomor CAS | 7782-49-2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sejarah | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Penamaan | dari Selene, dewi bulan Yunani | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Penemuan dan isolasi pertama | J. Berzelius dan Johann G. Gahn (1817) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Isotop selenium yang utama | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||
Selenium adalah sebuah unsur kimia dengan lambang Se dan nomor atom 34. Ia merupakan sebuah unsur nonlogam (lebih jarang dianggap sebagai metaloid) dengan sifat-sifat perantara antara unsur-unsur di atas dan di bawahnya dalam tabel periodik, belerang dan telurium, dan juga memiliki kemiripan dengan arsen. Ia jarang terjadi dalam keadaan elementalnya atau sebagai senyawa bijih murni di kerak Bumi. Selenium (dari bahasa Yunani Kuno σελήνη (selḗnē), berarti "bulan") ditemukan pada tahun 1817 oleh Jöns J. Berzelius, yang mencatat kemiripan unsur baru tersebut dengan telurium yang ditemukan sebelumnya (dinamai dari Bumi).
Selenium ditemukan dalam bijih logam sulfida, di mana ia sebagian menggantikan belerang. Secara komersial, selenium diproduksi sebagai produk sampingan dalam pemurnian bijih-bijih ini, paling sering selama produksi. Mineral yang merupakan senyawa selenida atau selenat murni telah diketahui tetapi langka. Penggunaan komersial utama untuk selenium saat ini adalah pembuatan kaca dan pigmen. Selenium adalah sebuah semikonduktor dan digunakan dalam fotosel. Aplikasinya dalam elektronika, dulunya penting, tetapi saat ini sebagian besar telah diganti dengan perangkat semikonduktor silikon. Selenium masih digunakan dalam beberapa jenis pelindung lonjakan daya DC dan satu jenis quantum dot fluoresen.
Meskipun selenium dalam jumlah kecil diperlukan untuk fungsi seluler pada banyak hewan, termasuk manusia, selenium elemental dan (terutama) garam selenium bersifat racun bahkan dalam dosis kecil, menyebabkan selenosis. Selenium terdaftar sebagai bahan dalam banyak multivitamin dan suplemen makanan lainnya, serta dalam susu formula bayi, dan merupakan komponen enzim antioksidan glutationa peroksidase dan tioredoksin reduktase (yang secara tidak langsung mengurangi molekul teroksidasi tertentu pada hewan dan beberapa tumbuhan) serta dalam 3 enzim deiodinase. Kebutuhan selenium pada tumbuhan berbeda menurut spesies, dengan beberapa tumbuhan membutuhkan jumlah yang relatif besar dan yang lainnya tampaknya tidak membutuhkannya.[6]
Karakteristik
[sunting | sunting sumber]Sifat fisik
[sunting | sunting sumber]
Selenium membentuk beberapa alotrop yang berinterkonversi dengan perubahan suhu, agak bergantung pada laju perubahan suhu. Ketika disiapkan dalam reaksi kimia, selenium biasanya berupa bubuk amorf berwarna merah bata. Ketika melebur dengan cepat, ia akan membentuk bentuk seperti kaca berwarna hitam, biasanya dijual secara komersial sebagai manik-manik.[7] Struktur selenium hitam tidaklah teratur dan kompleks serta terdiri dari cincin polimer dengan hingga 1000 atom per cincin. Se hitam adalah padatan rapuh dan berkilau yang sedikit larut dalam CS2. Saat dipanaskan, ia akan melunak pada suhu 50 °C dan berubah menjadi selenium abu-abu pada suhu 180 °C; suhu transformasinya akan berkurang dengan adanya halogen dan amina.[8]
Bentuk α, β, dan γ merah dihasilkan dari larutan selenium hitam dengan memvariasikan laju penguapan pelarut (biasanya CS2). Mereka semua memiliki simetri kristal monoklinik yang relatif rendah (grup ruang 14) dan mengandung cincin siklooktaselenium (Se8) berkerut yang hampir identik dengan susunan geometris yang berbeda, seperti pada belerang.[9] Delapan atom dari cincin tersebut tidaklah setara (yaitu mereka tidak dipetakan satu sama lain oleh operasi simetri apa pun), dan sebenarnya dalam bentuk γ-monoklinik, setengah dari cincin tersebut berada dalam satu konfigurasi (dan bayangan cerminnya) dan setengah lagi dalam konfigurasi lainnya.[10][11] Pengepakan paling padat dalam bentuk α. Pada cincin Se8, jarak Se-Se bervariasi tergantung di mana pasangan atom berada di dalam cincin, tetapi rata-ratanya adalah 233,5 pm, dan sudut Se-Se-Se berada pada rata-rata 105,7°. Alotrop selenium lainnya mungkin mengandung cincin Se6 atau Se7.[8]
Bentuk selenium yang paling stabil dan padat adalah bentuk abu-abu dan memiliki kisi kristal heksagon kiral (grup ruang 152 atau 154 tergantung pada kiralitas)[12] yang terdiri dari rantai polimer heliks, dimana jarak Se-Se adalah 237,3 pm dan sudut Se-Se-Se adalah 103,1° . Jarak minimum antar rantai adalah 343,6 pm. Se abu-abu dibentuk melalui pemanasan ringan alotrop lainnya, dengan pendinginan Se cair secara lambat, atau dengan mengembunkan uap Se tepat di bawah titik leburnya. Walaupun bentuk Se lainnya merupakan insulator, Se abu-abu adalah semikonduktor yang menunjukkan fotokonduktivitas yang cukup besar. Berbeda dengan alotrop lainnya, ia tidak larut dalam CS2.[8] Ia akan menolak oksidasi melalui udara dan tidak akan diserang oleh asam nonoksidator. Dengan agen pereduksi yang kuat, ia membentuk poliselenida. Selenium tidak menunjukkan perubahan viskositas yang dialami belerang ketika dipanaskan secara bertahap.[7][13]
Isotop
[sunting | sunting sumber]Selenium memiliki tujuh isotop alami. Lima di antaranya, 74Se, 76Se, 77Se, 78Se, 80Se, bersifat stabil, dengan 80Se menjadi yang paling melimpah (49,6% kelimpahan alami). Yang juga terjadi secara alami adalah radionuklida primordial 82Se, dengan waktu paruh 9,2×1019 tahun.[14] Radioisotop nonprimordial 79Se juga terdapat dalam jumlah kecil dalam bijih uranium sebagai produk fisi nuklir. Selenium juga memiliki banyak isotop sintetis yang tidak stabil mulai dari 64Se hingga 95Se; yang paling stabil adalah 75Se dengan waktu paruh 119,78 hari dan 72Se dengan waktu paruh 8,4 hari.[14] Isotop yang lebih ringan dari isotop stabil mengalami peluruhan beta plus menjadi isotop arsen, dan isotop yang lebih berat daripada isotop stabil mengalami peluruhan beta minus menjadi isotop bromin, dengan beberapa cabang emisi neutron kecil dalam isotop terberat yang diketahui.
| Isotop | Kealamian | Asal | Waktu paruh |
|---|---|---|---|
| 74Se | Primordial | Stabil | |
| 76Se | Primordial | Stabil | |
| 77Se | Primordial | Produk fisi | Stabil |
| 78Se | Primordial | Produk fisi | Stabil |
| 79Se | Renik | Produk fisi | 327.000 tahun[15][16] |
| 80Se | Primordial | Produk fisi | Stabil |
| 82Se | Primordial | Produk fisi* | ~1020 tahun[14][a] |
Senyawa
[sunting | sunting sumber]Senyawa selenium umumnya eksis pada keadaan oksidasi −2, +2, +4, dan +6.
Senyawa kalkogen
[sunting | sunting sumber]
Selenium membentuk dua oksida: selenium dioksida (SeO2) dan selenium trioksida (SeO3). Selenium dioksida dibentuk melalui reaksi selenium elemental dengan oksigen:[7]
Ia adalah padatan polimer yang membentuk molekul SeO2 monomer dalam fase gas. Ia akan larut dalam air untuk membentuk asam selenit, H2SeO3. Asam selenit juga dapat dibuat langsung melalui oksidasi selenium elemental dengan asam nitrat:[17]
Tidak seperti belerang, yang dapat membentuk trioksida yang stabil, selenium trioksida tidak stabil secara termodinamika dan akan terurai menjadi selenium dioksida di atas suhu 185 °C:[7][17]
- (ΔH = −54 kJ/mol)
Selenium trioksida diproduksi di laboratorium melalui reaksi belerang trioksida (SO3) dan kalium selenat (K2SeO4) anhidrat.[18]
Garam asam selenit disebut selenit. Contohnya adalah perak selenit (Ag2SeO3) dan natrium selenit (Na2SeO3).
Hidrogen sulfida bereaksi dengan asam selenit encer untuk menghasilkan selenium disulfida:
Selenium disulfida terdiri dari cincin beranggota-8. Ia memiliki komposisi perkiraan SeS2, dengan cincin individual bervariasi dalam komposisi, seperti Se4S4 dan Se2S6. Selenium disulfida telah digunakan dalam sampo sebagai agen antiketombe, penghambat dalam kimia polimer, pewarna kaca, dan agen pereduksi dalam kembang api.[17]
Selenium trioksida dapat disintesis dengan mendehidrasi asam selenat, H2SeO4, yang dihasilkan dari oksidasi selenium dioksida dengan hidrogen peroksida:[19]
Asam selenat pekat yang panas dapat bereaksi dengan emas untuk membentuk emas(III) selenat (Au2(SeO4)3).[20]
Senyawa halogen
[sunting | sunting sumber]Iodida selenium tidak dikenal dengan baik. Satu-satunya klorida yang stabil adalah selenium monoklorida (Se2Cl2), yang mungkin lebih dikenal sebagai selenium(I) klorida; bromida yang sesuai juga diketahui. Spesies ini secara struktural analog dengan disulfur diklorida yang sesuai. Selenium diklorida adalah reagen penting dalam pembuatan senyawa selenium (misalnya pembuatan Se7). Ia dibuat dengan mencampur selenium dengan sulfuril klorida (SO2Cl2).[21] Selenium akan bereaksi dengan fluorin untuk membentuk selenium heksafluorida:
Dibandingkan dengan rekan belerangnya (belerang heksafluorida), selenium heksafluorida (SeF6) lebih reaktif dan merupakan iritan paru-paru yang beracun.[22] Beberapa selenium oksihalida, seperti seleninil fluorida (SeOF2) dan selenium oksiklorida (SeOCl2) telah digunakan sebagai pelarut khusus.[7]
Selenida
[sunting | sunting sumber]Serupa dengan perilaku kalkogen lainnya, selenium membentuk hidrogen selenida, H2Se. Ia adalah gas yang sangat berbau, beracun, dan tidak berwarna. Ia lebih asam daripada hidrogen sulfida, H2S. Dalam larutan, ia akan terionisasi menjadi HSe−. Dianion selenida Se2− membentuk berbagai senyawa, termasuk mineral dari mana selenium diperoleh secara komersial. Selenida ilustrasif meliputi raksa selenida (HgSe), timbal selenida (PbSe), seng selenida (ZnSe), dan tembaga indium galium diselenida (Cu(Ga,In)Se2). Bahan-bahan ini adalah semikonduktor. Dengan logam yang sangat elektropositif, seperti aluminium, selenida-selenida ini rentan terhadap hidrolisis:[7]
Selenida logam alkali akan bereaksi dengan selenium untuk membentuk poliselenida, Se2−n, yang eksis sebagai rantai.
Senyawa lainnya
[sunting | sunting sumber]Tetraselenium tetranitrida, Se4N4, adalah sebuah senyawa berwarna oranye eksplosif yang analog dengan tetrasulfur tetranitrida (S4N4).[7][23][24] Ia dapat disintesis melalui reaksi selenium tetraklorida (SeCl4) dengan [((CH3)3Si)2N]2Se.[25]
Selenium akan bereaksi dengan sianida untuk menghasilkan selenosianat:[7]
Senyawa organoselenium
[sunting | sunting sumber]Selenium, terutama dalam keadaan oksidasi II, membentuk ikatan stabil dengan karbon, yang secara struktural analog dengan senyawa organobelerang yang sesuai. Yang paling umum adalah selenida (R2Se, analog tioeter), diselenida (R2Se2, analog disulfida), dan selenol (RSeH, analog tiol). Perwakilan selenida, diselenida, dan selenol masing-masing meliputi selenometionina, difenildiselenida, dan benzenaselenol. Sulfoksida dalam kimia belerang diwakili oleh selenoksida (rumus RSe(O)R) dalam kimia selenium, yang merupakan zat antara dalam sintesis organik, seperti yang diilustrasikan melalui reaksi eliminasi selenoksida. Konsisten dengan tren yang ditunjukkan oleh aturan ikatan ganda, selenoketon, R(C=Se)R, dan selenaldehida, R(C=Se)H, jarang teramati.[26]
Sejarah
[sunting | sunting sumber]Selenium (bahasa Yunani: σελήνη selene berarti "Bulan") ditemukan pada tahun 1817 oleh Jöns J. Berzelius dan Johan G. Gahn.[27] Kedua kimiawan tersebut memiliki pabrik kimia di dekat Gripsholm, Swedia, yang memroduksi asam sulfat melalui proses kamar timbal. Pirit dari Tambang Falun menciptakan endapan merah di kamar timbal yang dianggap sebagai senyawa arsen, sehingga penggunaan pirit untuk membuat asam dihentikan. Berzelius dan Gahn ingin menggunakan pirit dan mereka juga mengamati bahwa endapan merah mengeluarkan bau seperti lobak pedas saat dibakar. Bau ini tidak khas untuk arsen, tetapi bau serupa diketahui dari senyawa telurium. Oleh karena itu, surat pertama Berzelius kepada Alexander Marcet menyatakan bahwa ini adalah senyawa telurium. Namun, kurangnya senyawa telurium dalam mineral Tambang Falun akhirnya membuat Berzelius menganalisis ulang endapan merah tersebut, dan pada tahun 1818 dia menulis surat kedua kepada Marcet yang menjelaskan unsur yang baru ditemukan itu mirip dengan belerang dan telurium. Karena kemiripannya dengan telurium, yang dinamai dari Bumi, Berzelius menamai unsur baru itu dari Bulan.[28][29]
Pada tahun 1873, Willoughby Smith menemukan bahwa hambatan listrik dari selenium abu-abu bergantung pada cahaya sekitar.[30][31] Hal ini menyebabkan penggunaannya sebagai sel untuk menyensor cahaya. Produk komersial pertama yang menggunakan selenium dikembangkan oleh Werner Siemens pada pertengahan tahun 1870-an. Sel selenium digunakan dalam fotofon yang dikembangkan oleh Alexander G. Bell pada tahun 1879. Selenium mentransmisikan arus listrik sebanding dengan jumlah cahaya yang jatuh di permukaannya. Fenomena ini digunakan dalam desain pengukur cahaya dan perangkat serupa. Sifat semikonduktor selenium memiliki banyak aplikasi lain dalam elektronika.[32][33][34] Pengembangan penyearah selenium dimulai pada awal 1930-an, dan mereka menggantikan penyearah tembaga oksida karena mereka lebih efisien.[35][36][37] Mereka bertahan dalam aplikasi komersial hingga tahun 1970-an, setelah mereka diganti dengan penyearah silikon yang lebih murah dan bahkan lebih efisien.
Selenium kemudian menjadi perhatian medis karena toksisitasnya terhadap pekerja industri. Selenium juga diakui sebagai toksin hewan yang penting, yang terlihat pada hewan yang memakan tumbuhan tinggi selenium. Pada tahun 1954, petunjuk pertama tentang fungsi biologis spesifik dari selenium ditemukan pada mikroorganisme oleh ahli biokimia Jane Pinsent.[38][39] Ia ditemukan penting untuk kehidupan mamalia pada tahun 1957.[40][41] Pada tahun 1970-an, ia terbukti hadir dalam dua set enzim independen. Ini diikuti oleh penemuan selenosisteina dalam protein. Selama tahun 1980-an, selenosisteina terbukti dikodekan oleh kodon UGA. Mekanisme pengodean ulang pertama kali dilakukan pada bakteri dan kemudian pada mamalia (lihat unsur SECIS).[42]
Keterjadian
[sunting | sunting sumber]
Selenium asli (elemental) adalah sebuah mineral langka, yang biasanya tidak membentuk kristal yang baik, tetapi, jika terbentuk, mereka berstruktur rombohedra curam atau kristal berbentuk seperti jarum (seperti rambut) kecil.[43] Isolasi selenium seringkali dipersulit oleh adanya senyawa dan unsur lain.
Selenium terjadi secara alami dalam sejumlah bentuk anorganik, meliputi selenida, selenat, dan selenit, tetapi mineral ini jarang ditemukan. Mineral selenit yang umum bukanlah mineral selenium, dan tidak mengandung ion selenit, melainkan sejenis gipsum (kalsium sulfat hidrat) yang dinamai dari Bulan seperti selenium, jauh sebelum penemuan selenium. Selenium paling sering ditemukan sebagai pengotor, menggantikan sebagian kecil belerang dalam bijih sulfida dari banyak logam.[44][45]
Dalam sistem kehidupan, selenium ditemukan dalam asam amino selenometionina, selenosisteina, dan metilselenosisteina. Dalam senyawa ini, selenium memainkan peran yang analog dengan belerang. Senyawa organoselenium alami lainnya adalah dimetil selenida.[46][47]
Tanah tertentu kaya akan selenium, dan selenium dapat dibiokonsentrasikan oleh beberapa tumbuhan. Di tanah, selenium paling sering terjadi dalam bentuk larut seperti selenat (analog dengan sulfat), yang sangat mudah larut ke sungai oleh limpasan.[44][45] Air laut mengandung selenium dalam jumlah yang signifikan.[48][49]
Konsentrasi latar belakang khas selenium tidak melebihi 1 ng/m3 di atmosfer; 1 mg/kg di tanah dan tumbuh-tumbuhan, dan 0,5 μg/L di air tawar dan air laut.[50]
Sumber antropogenik selenium meliputi pembakaran batu bara, serta penambangan dan peleburan bijih sulfida.[51]
Produksi
[sunting | sunting sumber]Selenium paling sering diproduksi dari selenida di banyak bijih sulfida, seperti tembaga, nikel, atau timbal. Pemurnian logam elektrolitis sangatlah produktif selenium sebagai produk sampingan, diperoleh dari lumpur anoda kilang tembaga. Sumber lainnya adalah lumpur dari kamar timbal pabrik asam sulfat, sebuah proses yang tidak lagi digunakan. Selenium dapat disuling dari lumpur ini melalui sejumlah metode. Namun, sebagian besar selenium elemental hadir sebagai produk sampingan dari pemurnian tembaga atau produksi asam sulfat.[52][53] Sejak penemuannya, produksi tembaga melalui ekstraksi pelarut dan elektrodeposisi (SX/EW) telah meningkatkan pasokan tembaga di seluruh dunia.[54] Ini telah mengubah ketersediaan selenium, karena hanya sebagian kecil selenium dalam bijih yang terlindi dengan tembaga.[55]
Produksi industri selenium biasanya melibatkan ekstraksi selenium dioksida dari residu yang diperoleh selama pemurnian tembaga. Produksi umum dari residu tersebut kemudian dimulai dengan oksidasi dengan natrium karbonat untuk menghasilkan selenium dioksida, yang dicampur dengan air dan diasamkan untuk membentuk asam selenit (tahap oksidasi). Asam selenit kemudian digelembungkan dengan belerang dioksida (tahap reduksi) untuk menghasilkan selenium elemental.[56][57]
Sekitar 2.000 ton selenium diproduksi pada tahun 2011 di seluruh dunia, sebagian besar di Jerman (650 t), Jepang (630 t), Belgia (200 t), dan Rusia (140 t), dan total cadangan selenium diperkirakan mencapai 93.000 ton. Data ini mengecualikan dua produsen utama: Amerika Serikat dan Tiongkok. Kenaikan tajam sebelumnya diamati pada tahun 2004 dari AS$4–AS$5 menjadi AS$27/lb. Harganya relatif stabil selama tahun 2004–2010 pada sekitar AS$30 per pon (dalam lot 100 pon) tetapi meningkat menjadi AS$65/lb pada tahun 2011. Konsumsi selenium pada tahun 2010 dibagi sebagai berikut: metalurgi – 30%, manufaktur kaca – 30%, pertanian – 10%, bahan kimia dan pigmen – 10%, dan elektronika – 10%. Tiongkok adalah konsumen selenium yang dominan, dengan jumlah 1.500–2.000 ton/tahun.[58]
Aplikasi
[sunting | sunting sumber]Pupuk
[sunting | sunting sumber]Peneliti menemukan bahwa penerapan pupuk selenium pada tanaman selada dapat menurunkan akumulasi timbal dan kadmium. Persik dan pir yang diberi semprotan selenium akan mengandung kadar selenium yang lebih tinggi serta tetap kokoh dan matang lebih lama saat disimpan. Dalam dosis rendah, selenium telah menunjukkan efek menguntungkan pada ketahanan tumbuhan terhadap berbagai faktor tekanan lingkungan, meliputi kekeringan, UV-B, keasinan tanah, dan suhu dingin atau panas. Namun, ia dapat merusak tumbuhan pada dosis yang lebih tinggi.[59]
Elektrolisis mangan
[sunting | sunting sumber]Selama elektrodeposisi mangan, penambahan selenium dioksida menurunkan daya yang diperlukan untuk mengoperasikan sel elektrolisis. Tiongkok adalah konsumen terbesar selenium dioksida untuk tujuan ini. Untuk setiap ton mangan, rata-rata digunakan 2 kg selenium oksida.[58][60]
Produksi kaca
[sunting | sunting sumber]Penggunaan komersial terbesar Se, terhitung sekitar 50% dari total konsumsi, adalah untuk produksi kaca. Senyawa Se memberi warna merah pada kaca. Warna ini meniadakan semburat hijau atau kuning yang muncul dari kotoran besi yang khas pada kebanyakan kaca. Untuk tujuan ini, berbagai garam selenit dan selenat ditambahkan. Untuk aplikasi lain, warna merah mungkin diinginkan, yang dihasilkan oleh campuran CdSe dan CdS.[61]
Paduan
[sunting | sunting sumber]Selenium digunakan dengan bismut pada kuningan untuk menggantikan timbal yang lebih beracun. Regulasi timbal dalam aplikasi air minum seperti di A.S. dengan Undang-undang Air Minum Aman tahun 1974, membuat pengurangan timbal dalam kuningan diperlukan. Kuningan baru dipasarkan dengan nama EnviroBrass.[62] Seperti timbal dan belerang, selenium dapat meningkatkan kemampuan pemesinan baja pada konsentrasi sekitar 0,15%.[63][64] Selenium menghasilkan peningkatan pemesinan yang sama pada paduan tembaga.[65]
Baterai litium–selenium
[sunting | sunting sumber]Baterai litium–selenium (Li–Se) adalah salah satu sistem yang paling menjanjikan untuk penyimpanan energi dalam keluarga baterai litium.[66] Baterai Li–Se adalah alternatif dari baterai litium–belerang, dengan keunggulan konduktivitas listrik yang tinggi.
Sel surya
[sunting | sunting sumber]Selenium adalah dasar dari sel surya pertama, dengan contoh pertama dari sel surya atap adalah sel selenium dari tahun 1884. Sel tersebut kemudian digunakan dalam pengukur cahaya bebas-baterai untuk fotografi. Tembaga indium galium selenida adalah bahan yang digunakan dalam sel surya.[67]
Fotokonduktor
[sunting | sunting sumber]Film tipis selenium amorf (Se-α) telah memiliki aplikasi sebagai fotokonduktor dalam pendeteksi sinar-X panel datar. Pendeteksi ini menggunakan selenium amorf untuk menangkap dan mengubah foton sinar-X insiden langsung menjadi muatan listrik. Selenium telah dipilih untuk aplikasi ini di antara semikonduktor lainnya karena kombinasi sifat teknologi dan fisiknya yang menguntungkan:[68][69]
- Selenium amorf memiliki titik lebur rendah, tekanan uap tinggi, dan struktur yang seragam. Ketiga sifat ini memungkinkan deposisi film seragam area-besar dengan cepat dan mudah dengan ketebalan hingga 1 mm pada laju 1–5 µm/menit. Keseragaman dan kurangnya batas butir, yang intrinsik untuk bahan polikristalin, akan meningkatkan kualitas gambar sinar-X. Sedangkan area yang luas sangat penting untuk memindai tubuh manusia atau barang bawaan.
- Selenium kurang beracun daripada banyak senyawa semikonduktor yang mengandung arsen atau logam berat seperti raksa atau timbal.
- Mobilitasnya dalam medan listrik terapan cukup tinggi baik untuk elektron maupun lubang, sehingga pada perangkat setebal 0,2 mm, sekitar 98% elektron dan lubang yang dihasilkan oleh sinar-X akan terkumpul di elektroda tanpa terperangkap oleh berbagai cacat. Konsekuensinya, sensitivitas perangkatnya tinggi, dan perilakunya mudah dijelaskan dengan persamaan transportasi sederhana.
Penyearah
[sunting | sunting sumber]Penyearah selenium pertama kali digunakan pada tahun 1933. Penggunaannya berlanjut hingga tahun 1990-an.
Kegunaan lainnya
[sunting | sunting sumber]Sejumlah kecil senyawa organoselenium telah digunakan untuk memodifikasi katalis yang digunakan untuk vulkanisasi produksi karet.[55]
Permintaan selenium oleh industri elektronika semakin menurun.[58] Sifat fotovoltaik dan fotokonduktifnya masih berguna dalam fotokopi,[70][71][72][73] fotosel, pengukur cahaya, dan sel surya. Penggunaannya sebagai fotokonduktor pada mesin fotokopi kertas kosong pernah menjadi aplikasi utama, tetapi pada 1980-an, aplikasi fotokonduktornya menurun (walaupun ia masih merupakan penggunaan akhir yang besar) karena semakin banyak mesin fotokopi beralih ke fotokonduktor organik. Meskipun pernah digunakan secara luas, penyearah selenium sebagian besar telah digantikan (atau sedang digantikan) oleh perangkat berbasis silikon. Pengecualian yang paling menonjol adalah perlindungan lonjakan daya DC, di mana kemampuan energi superior dari penekan selenium membuatnya lebih diinginkan daripada varistor logam-oksida.
Seng selenida adalah bahan pertama untuk LED biru, tetapi galium nitrida mendominasi pasar tersebut.[74] Kadmium selenida adalah komponen penting dalam quantum dot. Lembaran selenium amorf mengubah gambar sinar-X menjadi pola muatan dalam xeroradiografi dan dalam kamera sinar-X panel datar bahan padat.[75] Selenium terionisasi (Se+24[butuh klarifikasi]) adalah salah satu media aktif yang digunakan dalam laser sinar-X.[76]
Selenium adalah katalis dalam beberapa reaksi kimia, tetapi tidak banyak digunakan karena masalah toksisitas.[77] Dalam kristalografi sinar-X, penggabungan satu atau lebih atom selenium sebagai pengganti belerang akan membantu dengan penahapan dispersi anomali panjang gelombang ganda dan dispersi anomali panjang gelombang tunggal.[78]
Selenium digunakan dalam pewarnaan cetakan fotografi, dan dijual sebagai toner oleh banyak produsen fotografi. Selenium mengintensifkan dan memperluas jangkauan tonal dari gambar fotografi hitam-putih dan meningkatkan ketahanan cetakan.[79][80][81]
75Se digunakan sebagai sumber gama dalam radiografi industri.[82]
Selenium digunakan pada beberapa sampo antiketombe dalam bentuk selenium disulfida seperti merek Selsun dan Vichy Dereos.[83]
Pencemaran
[sunting | sunting sumber]Dalam konsentrasi tinggi, selenium bertindak sebagai kontaminan lingkungan. Sumber polusinya meliputi bahan limbah dari operasi pertambangan, pertanian, petrokimia, dan manufaktur industri tertentu. Di Danau Belews, Carolina Utara, 19 spesies ikan tersingkir dari danau karena 150–200 μg Se/L air limbah dibuang dari tahun 1974 hingga 1986 dari pembangkit listrik tenaga batu bara Duke Energy. Di Suaka Margasatwa Nasional Kesterson di California, ribuan ikan dan burung air diracuni oleh selenium dalam drainase irigasi pertanian.
Pencemaran selenium mungkin berdampak pada beberapa sistem perairan dan mungkin disebabkan oleh faktor antropogenik seperti limpasan pertanian dan proses industri.[84] Orang yang makan lebih banyak ikan umumnya lebih sehat daripada mereka yang makan lebih sedikit,[85] yang menunjukkan tidak ada masalah kesehatan utama manusia dari polusi selenium, meskipun selenium memiliki efek potensial pada manusia.[86]
Perubahan fisiologis substansial dapat terjadi pada ikan dengan konsentrasi jaringan selenium yang tinggi. Ikan yang terkena selenium dapat mengalami pembengkakan pada lamela insang, yang menghambat difusi oksigen melintasi insang dan aliran darah di dalam insang. Kapasitas pernapasan semakin berkurang karena selenium mengikat hemoglobin. Masalah lainnya meliputi degenerasi jaringan hati, pembengkakan di sekitar jantung, kerusakan folikel telur di ovarium, katarak, dan penumpukan cairan di rongga tubuh dan kepala. Selenium sering menyebabkan janin ikan menjadi cacat yang mungkin mengalami masalah makan atau bernafas; distorsi sirip atau tulang belakang juga sering terjadi. Ikan dewasa mungkin tampak sehat meskipun tidak mampu menghasilkan keturunan yang layak.
Selenium terbioakumulasi di habitat perairan, yang menghasilkan konsentrasi yang lebih tinggi pada organisme daripada air di sekitarnya. Senyawa organoselenium dapat dipekatkan lebih dari 200.000 kali oleh zooplankton ketika konsentrasi air berada dalam kisaran 0,5 hingga 0,8 μg Se/L. Selenium anorganik lebih mudah terakumulasi dalam fitoplankton daripada zooplankton. Fitoplankton dapat mengkonsentrasikan selenium anorganik dengan faktor 3000. Konsentrasi lebih lanjut melalui bioakumulasi terjadi di sepanjang rantai makanan, karena predator memakan mangsa yang kaya selenium. Direkomendasikan bahwa konsentrasi air 2 μg Se/L dianggap sangat berbahaya bagi ikan sensitif dan burung air. Keracunan selenium dapat diturunkan dari induk kepada keturunannya melalui telur, dan keracunan selenium dapat bertahan selama beberapa generasi. Reproduksi itik melewar akan terganggu pada konsentrasi makanan 7 μg Se/L. Banyak invertebrata bentik dapat mentolerir konsentrasi selenium hingga 300 μg/L Se dalam makanannya.[87]
Bioakumulasi selenium di lingkungan perairan dapat menyebabkan kematian ikan tergantung pada spesies di daerah yang terkena. Namun, ada beberapa spesies yang terlihat bertahan dari peristiwa ini dan mentolerir peningkatan selenium. Juga diperkirakan bahwa musim dapat berdampak pada efek berbahaya selenium pada ikan.[88]
Keracunan selenium pada sistem air dapat terjadi setiap kali aliran limpasan pertanian baru melintas melalui lahan kering. Proses ini melepaskan senyawa selenium alami yang larut (seperti selenat) ke dalam air, yang kemudian terkonsentrasi di lahan basah saat air menguap. Pencemaran selenium pada saluran air juga terjadi ketika selenium terlindi dari abu cerobong batu bara, pertambangan dan peleburan logam, pemrosesan minyak mentah, dan tempat pembuangan sampah.[89] Tingkat selenium yang tinggi di saluran air ditemukan dapat menyebabkan kelainan bawaan pada spesies ovipar, termasuk burung[90] dan ikan lahan basah.[91] Tingkat metilraksa makanan yang meningkat dapat memperkuat bahaya toksisitas selenium pada spesies ovipar.[92][93]
Peran biologis
[sunting | sunting sumber]| Bahaya |
|---|
Meskipun beracun dalam dosis besar, selenium merupakan mikronutrien penting bagi hewan. Pada tumbuhan, ia terjadi sebagai mineral pengamat,[94] kadang-kadang dalam proporsi beracun dalam hijauan (beberapa tumbuhan dapat mengakumulasi selenium sebagai pertahanan agar tidak dimakan oleh hewan,[95] tetapi tumbuhan lain, seperti rumput gila (locoweed), membutuhkan selenium, dan pertumbuhannya menunjukkan adanya selenium di tanah).[96]
Selenium adalah komponen dari asam amino selenosisteina dan selenometionina yang tidak biasa. Pada manusia, selenium merupakan unsur nutrien yang berfungsi sebagai kofaktor untuk reduksi enzim antioksidan, seperti glutationa peroksidase[97] dan bentuk tertentu dari tioredoksin reduktase dan beberapa tumbuhan (enzim ini terdapat pada semua organisme hidup, tetapi tidak semua bentuknya pada tumbuhan membutuhkan selenium).
Kelompok enzim glutationa peroksidase (GSH-Px) dapat mengatalisasi reaksi tertentu yang menghilangkan spesies oksigen reaktif seperti hidrogen peroksida dan hidroperoksida organik:
- 2 GSH + H2O2----GSH-Px → GSSG + 2 H2O
Kelenjar tiroid dan setiap sel yang menggunakan hormon tiroid menggunakan selenium,[98] yang merupakan kofaktor untuk tiga dari empat jenis deiodinase hormon tiroid yang diketahui, yang mengaktifkan dan kemudian menonaktifkan berbagai hormon tiroid dan metabolitnya; iodotironina deiodinase adalah subfamili dari enzim deiodinase yang menggunakan selenium sebagai asam amino selenosisteina yang jarang. (Hanya deiodinase iodotirosina deiodinase, yang bekerja pada produk penguraian terakhir dari hormon tiroid, yang tidak menggunakan selenium.)[99]
Selenium dapat menghambat penyakit Hashimoto, di mana sel tiroid tubuh sendiri diserang sebagai benda asing. Pengurangan 21% pada antibodi TPO dilaporkan dengan asupan makanan 0,2 mg selenium.[100]
Peningkatan selenium diet akan mengurangi efek toksisitas raksa,[101][102][103] meskipun hanya efektif pada dosis raksa rendah hingga sedang.[104] Bukti menunjukkan bahwa mekanisme molekuler dari toksisitas raksa mencakup penghambatan selenoenzim yang tidak dapat diubah yang diperlukan untuk mencegah dan membalikkan kerusakan oksidatif di otak dan jaringan endokrin.[105][106] Sebuah antioksidan, selenoneina, yang berasal dari selenium dan telah ditemukan hadir dalam darah tuna sirip biru, adalah subjek penelitian ilmiah mengenai kemungkinan perannya dalam penyakit inflamasi dan kronis, detoksifikasi metilraksa, dan kerusakan oksidatif.[107][108] Sepertinya ketika kadar raksa dalam ikan laut naik, maka kadar selenium juga akan naik. Sepengetahuan para peneliti, tidak ada laporan mengenai kadar raksa yang melebihi kadar selenium pada ikan laut.[109]
Evolusi dalam biologi
[sunting | sunting sumber]Sejak sekitar tiga miliar tahun yang lalu, keluarga selenoprotein prokariotik mendorong evolusi selenosisteina, sebuah asam amino. Selenium dimasukkan ke dalam beberapa keluarga selenoprotein prokariotik pada bakteri, arkea, dan eukariota sebagai selenosisteina,[110] di mana peroksiredoksin selenoprotein melindungi sel bakteri dan eukariotik terhadap kerusakan oksidatif. Keluarga selenoprotein dari GSH-Px dan deiodinase sel eukariotik tampaknya memiliki asal filogenetik bakteri. Bentuk yang mengandung selenosisteina terjadi pada spesies yang beragam seperti alga hijau, diatom, bulu babi, ikan, dan ayam. Enzim selenium terlibat dalam molekul pereduksi kecil glutationa dan tioredoksin. Satu keluarga molekul pengandung selenium (glutationa peroksidase) akan menghancurkan peroksida dan memperbaiki membran sel yang rusak akibat terperoksidasi, menggunakan glutationa. Enzim lain yang mengandung selenium pada beberapa tumbuhan dan hewan (tioredoksin reduktase) menghasilkan tioredoksin tereduksi, sebuah ditiol yang berfungsi sebagai sumber elektron untuk peroksidase dan juga ribonukleotida reduktase enzim pereduksi penting yang membuat prekursor DNA dari prekursor RNA.[111]
Unsur nutrien yang terlibat dalam aktivitas enzim GSH-Px dan superoksida dismutase, yaitu selenium, vanadium, magnesium, tembaga, dan seng, mungkin kurang di beberapa daerah yang kekurangan mineral terestrial.[110] Organisme laut mempertahankan dan terkadang memperluas selenoproteomnya, sedangkan selenoproteom dari beberapa organisme terestrial akan berkurang atau hilang sama sekali. Temuan ini menunjukkan bahwa, dengan pengecualian vertebrata, kehidupan akuatik mendukung penggunaan selenium, sedangkan habitat darat menyebabkan berkurangnya penggunaan unsur nutrien ini.[112] Ikan laut dan kelenjar tiroid vertebrata memiliki konsentrasi selenium dan iodin tertinggi. Sejak sekitar 500 juta tahun yang lalu, tumbuhan air tawar dan terestrial secara perlahan mengoptimalkan produksi antioksidan endogen "baru" seperti asam askorbat (vitamin C), polifenol (termasuk flavonoid), tokoferol, dll. Beberapa di antaranya muncul baru-baru ini, dalam 50–200 juta tahun terakhir, dalam buah-buahan dan bunga tumbuhan angiospermae. Faktanya, angiospermae (jenis tumbuhan yang dominan saat ini) dan sebagian besar pigmen antioksidannya berevolusi selama periode Jurasik akhir.[butuh rujukan]
Isoenzim deiodinase merupakan keluarga lain dari selenoprotein eukariotik dengan fungsi enzim yang teridentifikasi. Deiodinase mampu mengekstraksi elektron dari iodida, dan iodida dari iodotironin. Dengan demikian, mereka terlibat dalam pengaturan hormon tiroid, berpartisipasi dalam perlindungan tirosit dari kerusakan oleh H2O2 yang diproduksi untuk biosintesis hormon tiroid.[113] Sekitar 200 juta tahun lalu, selenoprotein baru dikembangkan sebagai enzim GSH-Px mamalia.[114][115][116][117]
Sumber nutrisi selenium
[sunting | sunting sumber]Selenium makanan berasal dari daging, kacang-kacangan, sereal, dan jamur. Kacang Brasil adalah sumber makanan terkaya (meskipun ini bergantung pada tanah, karena kacang Brasil tidak membutuhkan selenium tingkat tinggi untuk kebutuhannya sendiri).[118][119]
Angka Kecukupan Gizi (AKG) selenium yang direkomendasikan A.S. untuk remaja dan dewasa adalah 55 µg/hari. Selenium sebagai suplemen makanan tersedia dalam berbagai bentuk, meliputi suplemen multi-vitamin/mineral, yang biasanya mengandung 55 atau 70 µg/sajian. Suplemen khusus selenium biasanya mengandung 100 atau 200 µg/sajian.
Pada bulan Juni 2015, Badan Pengawas Obat dan Makanan (FDA) A.S. menerbitkan peraturan terakhirnya yang menetapkan persyaratan tingkat minimum dan maksimum selenium dalam susu formula.[120]
Kandungan selenium dalam tubuh manusia dipercaya berada pada kisaran 13–20 mg.[121]
Spesies tumbuhan indikator
[sunting | sunting sumber]Spesies tumbuhan tertentu dianggap sebagai indikator adanya kandungan selenium yang tinggi di tanah karena mereka membutuhkan kadar selenium yang tinggi untuk tumbuh subur. Tumbuhan indikator selenium utama adalah spesies Astragalus (termasuk beberapa rumput gila), Stanleya sp., aster kayu (Xylorhiza sp.), dan Oonopsis sp.[122]
Deteksi dalam cairan biologis
[sunting | sunting sumber]Selenium dapat diukur dalam darah, plasma, serum, atau urine untuk memantau paparan lingkungan atau pekerjaan yang berlebihan, untuk memastikan diagnosis keracunan pada korban yang dirawat di rumah sakit, atau menyelidiki dugaan kasus overdosis yang fatal. Beberapa teknik analitik mampu membedakan bentuk selenium organik dari anorganik. Bentuk selenium organik dan anorganik sebagian besar diubah menjadi konjugat monosakarida (selenosugar) dalam tubuh sebelum dibuang melalui urine. Pasien kanker yang menerima selenotionina dosis oral setiap hari dapat mencapai konsentrasi selenium plasma dan urine yang sangat tinggi.[123]
Toksisitas
[sunting | sunting sumber]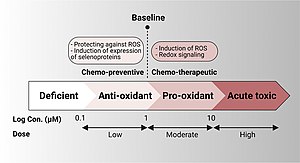
Meskipun selenium merupakan unsur nutrien yang penting, ia bersifat racun jika dikonsumsi secara berlebihan. Melebihi Batas Atas Asupan sebesar 400 mikrogram per hari dapat menyebabkan selenosis.[125] Batas Atas Asupan 400 µg ini didasarkan terutama pada penelitian tahun 1986 terhadap lima pasien Tiongkok yang menunjukkan tanda-tanda selenosis yang nyata dan penelitian lanjutan pada lima orang yang sama pada tahun 1992.[126] Penelitian tahun 1992 benar-benar menemukan bahwa asupan Se makanan yang paling aman adalah sekitar 800 mikrogram per hari (15 mikrogram per kilogram berat badan), tetapi disarankan 400 mikrogram per hari untuk menghindari ketidakseimbangan nutrisi dalam makanan dan sesuai dengan data dari negara lain.[127] Di Tiongkok, orang yang menelan jagung yang tumbuh di batu bara yang kaya selenium (batu serpih yang mengandung karbon) menderita keracunan selenium. Batu bara ini terbukti memiliki kandungan selenium setinggi 9,1%, konsentrasi tertinggi dalam batu bara yang pernah tercatat.[128]
Tanda dan gejala selenosis meliputi bau bawang putih pada napas, gangguan pencernaan, rambut rontok, pengelupasan kuku, kelelahan, mudah tersinggung, dan kerusakan saraf. Kasus ekstrem selenosis dapat menunjukkan sirosis hati, edema paru-paru, atau bahkan kematian.[129] Selenium elemental dan sebagian besar selenida metalik memiliki toksisitas yang relatif rendah karena bioavailabilitasnya rendah. Sebaliknya, selenat dan selenit memiliki sebuah mode aksi oksidan yang serupa dengan arsen trioksida dan sangat beracun. Dosis selenit toksik kronis bagi manusia adalah sekitar 2400 hingga 3000 mikrogram selenium per hari.[130] Hidrogen selenida adalah sebuah gas korosif yang sangat beracun.[131] Selenium juga terdapat dalam senyawa organik, seperti dimetil selenida, selenometionina, selenosisteina, dan metilselenosisteina, yang semuanya memiliki bioavailabilitas tinggi dan beracun dalam dosis besar.
Pada 19 April 2009, 21 kuda poni polo mati sesaat sebelum pertandingan di Polo Terbuka Amerika Serikat. Tiga hari kemudian, sebuah apotek mengeluarkan pernyataan yang menjelaskan bahwa kuda-kuda tersebut telah menerima dosis yang salah dari salah satu bahan yang digunakan dalam senyawa suplemen vitamin/mineral yang telah disiapkan secara tidak benar oleh apotek peracikan. Analisis kadar senyawa anorganik dalam suplemen tersebut menunjukkan konsentrasi selenium 10 hingga 15 kali lebih tinggi dari kadar normal dalam sampel darah, dan 15 hingga 20 kali lebih tinggi dari kadar normal dalam sampel hati. Selenium kemudian dipastikan sebagai faktor toksik.[132]

Pada ikan dan satwa liar lainnya, selenium diperlukan untuk kehidupan, tetapi beracun dalam dosis tinggi. Untuk ikan salmon, konsentrasi selenium yang optimal adalah sekitar 1 mikrogram selenium per gram berat badan keseluruhan. Jauh di bawah level itu, salmon muda akan mati karena kekurangan;[134] jauh di atas, mereka akan mati karena kelebihan racun.[133]
Administrasi Keselamatan dan Kesehatan Kerja (OSHA) telah menetapkan batas legal (batas paparan yang diizinkan) untuk selenium di tempat kerja sebesar 0,2 mg/m3 selama 8 jam hari kerja. Institut Nasional untuk Keselamatan dan Kesehatan Kerja (NIOSH) telah menetapkan batas paparan yang direkomendasikan (REL) sebesar 0,2 mg/m3 selama 8 jam hari kerja. Pada kadar 1 mg/m3, selenium langsung berbahaya bagi kehidupan dan kesehatan.[136]
Kekurangan selenium
[sunting | sunting sumber]Kekurangan selenium dapat terjadi pada pasien dengan fungsi pencernaan yang sangat terganggu, mereka yang menjalani nutrisi parenteral total, dan[137] pada mereka yang berusia lanjut (di atas 90). Juga, orang yang bergantung pada makanan yang tumbuh dari tanah yang kekurangan selenium juga berisiko. Meskipun tanah Selandia Baru memiliki tingkat selenium yang rendah, efek kesehatan yang merugikan belum terdeteksi pada penduduknya.[138]
Kekurangan selenium, yang ditentukan oleh tingkat aktivitas selenoenzim yang rendah (<60% dari normal) di otak dan jaringan endokrin, terjadi hanya ketika tingkat selenium yang rendah dikaitkan dengan stres tambahan, seperti paparan raksa yang tinggi[139] atau peningkatan stres oksidan akibat kekurangan vitamin E.[140]
Selenium berinteraksi dengan nutrisi lain, seperti iodin dan vitamin E. Efek kekurangan selenium pada kesehatan masih belum jelas, terutama terkait dengan penyakit Kashin–Beck.[141] Selenium juga berinteraksi dengan mineral lain, seperti seng dan tembaga. Suplemen selenium dosis tinggi pada hewan hamil dapat mengganggu rasio seng:tembaga dan menyebabkan pengurangan seng; dalam kasus perawatan seperti itu, kadar seng harus dipantau. Penelitian lebih lanjut diperlukan untuk mengonfirmasi interaksi ini.[142]
Di beberapa daerah (misalnya berbagai daerah di Amerika Utara) di mana tingkat tanah selenium yang rendah akan menyebabkan konsentrasi rendah pada tumbuhan, beberapa spesies hewan mungkin akan kekurangan selenium kecuali selenium disuplementasi melalui makanan atau suntikan.[143] Ruminansia sangat rentan terhadap hal ini. Secara umum, penyerapan selenium makanan lebih rendah pada ruminansia daripada hewan lain, dan lebih rendah dari hijauan daripada dari biji-bijian.[144] Ruminansia yang merumput hijauan tertentu, misalnya, beberapa varietas semanggi putih yang mengandung glikosida sianogenik, mungkin memiliki kebutuhan selenium yang lebih tinggi,[144] mungkin karena sianida dilepaskan dari aglikona oleh aktivitas glukosidase dalam rumen[145] dan glutationa peroksidase dinonaktifkan oleh sianida yang bekerja pada moitas glutationa.[146] Neonatus ruminansia yang berisiko terkena penyakit otot putih dapat diberi selenium dan vitamin E melalui suntikan; beberapa miopati WMD hanya merespons selenium, beberapa hanya vitamin E, dan beberapa keduanya.[147]
Efek kesehatan
[sunting | sunting sumber]Efek asupan selenium pada kanker telah dipelajari dalam beberapa uji klinis dan penelitian epidemiologis pada manusia. Selenium mungkin memiliki peran kemopreventif dalam risiko kanker sebagai sebuah antioksidan, dan mungkin memicu respon imun. Pada tingkat rendah, ia digunakan dalam tubuh untuk membuat selenoprotein antioksidan, pada dosis yang lebih tinggi dari biasanya menyebabkan kematian sel.[124]
Selenium (dalam keterkaitan erat dengan iodin) berperan dalam kesehatan tiroid. Selenium adalah kofaktor untuk tiga deiodinase hormon tiroid, membantu mengaktifkan dan kemudian menonaktifkan berbagai hormon tiroid dan metabolitnya. Kekurangan selenium terisolasi sekarang sedang diselidiki karena perannya dalam reaksi autoimun induksi pada kelenjar tiroid pada penyakit Hashimoto.[148] Namun, dalam kasus kekurangan iodin dan selenium gabungan, kekurangan selenium terbukti berperan dalam melindungi tiroid.[149]
Lihat pula
[sunting | sunting sumber]Catatan
[sunting | sunting sumber]- ^ Untuk semua tujuan praktis, 82Se dianggap stabil.
Referensi
[sunting | sunting sumber]- ^ (Indonesia) "Selenium". KBBI Daring. Diakses tanggal 17 Juli 2022.
- ^ A Se(0) atom has been identified using DFT in [ReOSe(2-pySe)3]; see Cargnelutti, Roberta; Lang, Ernesto S.; Piquini, Paulo; Abram, Ulrich (2014). "Synthesis and structure of [ReOSe(2-Se-py)3]: A rhenium(V) complex with selenium(0) as a ligand". Inorganic Chemistry Communications. 45: 48–50. doi:10.1016/j.inoche.2014.04.003. ISSN 1387-7003.
- ^ Greenwood, Norman N.; Earnshaw, A. (1997), Chemistry of the Elements (edisi ke-2), Oxford: Butterworth-Heinemann, ISBN 0-7506-3365-4
- ^ Magnetic susceptibility of the elements and inorganic compounds, in Lide, D. R., ed. (2005). CRC Handbook of Chemistry and Physics (edisi ke-86). Boca Raton (FL): CRC Press. ISBN 0-8493-0486-5.
- ^ Weast, Robert (1984). CRC, Handbook of Chemistry and Physics. Boca Raton, Florida: Chemical Rubber Company Publishing. hlm. E110. ISBN 0-8493-0464-4.
- ^ Ruyle, George. "Poisonous Plants on Arizona Rangelands" (PDF). The University of Arizona. Diarsipkan dari versi asli (PDF) tanggal 15 Juli 2004. Diakses tanggal 28 Juni 2023.
- ^ a b c d e f g h House, James E. (2008). Inorganic chemistry. Academic Press. hlm. 524. ISBN 978-0-12-356786-4.
- ^ a b c Greenwood, Norman N.; Earnshaw, A. (1997), Chemistry of the Elements (edisi ke-2), Oxford: Butterworth-Heinemann, hlm. 751–752, ISBN 0-7506-3365-4
- ^ Olav Foss and Vitalijus Janickis (1980). "Crystal structure of γ-monoclinic selenium". Journal of the Chemical Society, Dalton Transactions (4): 624–627. doi:10.1039/DT9800000624.
- ^ "β –Se (Al ) Structure: A_mP32_14_8e". Encyclopedia of Crystallographic Prototypes.
- ^ "β –Se (Al ) Structure: A_mP32_14_16e". Encyclopedia of Crystallographic Prototypes.
- ^ "β –Se (Al ) Structure: A_hP3_152_a". Encyclopedia of Crystallographic Prototypes.
- ^ Video of selenium heating di YouTube
- ^ a b c Audi, G.; Kondev, F. G.; Wang, M.; Huang, W. J.; Naimi, S. (2017). "The NUBASE2016 evaluation of nuclear properties" (PDF). Chinese Physics C. 41 (3): 030001. Bibcode:2017ChPhC..41c0001A. doi:10.1088/1674-1137/41/3/030001.
- ^ "The half-life of 79Se". Physikalisch-Technische Bundesanstalt. 23 September 2010. Diakses tanggal 28 Juni 2023.
- ^ Jörg, Gerhard; Bühnemann, Rolf; Hollas, Simon; et al. (2010). "Preparation of radiochemically pure 79Se and highly precise determination of its half-life". Applied Radiation and Isotopes. 68 (12): 2339–2351. doi:10.1016/j.apradiso.2010.05.006. PMID 20627600.
- ^ a b c Wiberg, Egon; Wiberg, Nils; Holleman, Arnold Frederick (2001). Inorganic chemistry. San Diego: Academic Press. hlm. 583. ISBN 978-0-12-352651-9.
- ^ Greenwood, Norman N.; Earnshaw, A. (1997), Chemistry of the Elements (edisi ke-2), Oxford: Butterworth-Heinemann, hlm. 780, ISBN 0-7506-3365-4
- ^ Seppelt, K.; Desmarteau, Darryl D. (1980). Selenoyl difluoride. Inorganic Syntheses. 20. hlm. 36–38. doi:10.1002/9780470132517.ch9. ISBN 978-0-471-07715-2. Laporan tersebut menjelaskan sintesis asam selenat.
- ^ Lenher, V. (April 1902). "Action of selenic acid on gold". Journal of the American Chemical Society. 24 (4): 354–355. doi:10.1021/ja02018a005.
- ^ Xu, Zhengtao (2007). Devillanova, Francesco A., ed. Handbook of chalcogen chemistry: new perspectives in sulfur, selenium and tellurium. Royal Society of Chemistry. hlm. 460. ISBN 978-0-85404-366-8.
- ^ Proctor, Nick H.; Hathaway, Gloria J. (2004). Hughes, James P., ed. Proctor and Hughes' chemical hazards of the workplace (edisi ke-5). Wiley-IEEE. hlm. 625. ISBN 978-0-471-26883-3.
- ^ Woollins, Derek; Kelly, Paul F. (1993). "The Reactivity of Se4N4 in Liquid Ammonia". Polyhedron. 12 (10): 1129–1133. doi:10.1016/S0277-5387(00)88201-7.
- ^ Kelly, P.F.; Slawin, A.M.Z.; Soriano-Rama, A. (1997). "Use of Se4N4 and Se(NSO)2 in the preparation of palladium adducts of diselenium dinitride, Se2N2; crystal structure of [PPh4]2[Pd2Br6(Se2N2)]". Dalton Transactions (4): 559–562. doi:10.1039/a606311j.
- ^ Siivari, Jari; Chivers, Tristram; Laitinen, Risto S. (1993). "A simple, efficient synthesis of tetraselenium tetranitride". Inorganic Chemistry. 32 (8): 1519–1520. doi:10.1021/ic00060a031.
- ^ Erker, G.; Hock, R.; Krüger, C.; Werner, S.; Klärner, F.G.; Artschwager-Perl, U. (1990). "Synthesis and Cycloadditions of Monomeric Selenobenzophenone". Angewandte Chemie International Edition in English. 29 (9): 1067–1068. doi:10.1002/anie.199010671.
- ^ Berzelius, J.J. (1818). "Lettre de M. Berzelius à M. Berthollet sur deux métaux nouveaux" [Surat dari Tn. Berzelius kepada Tn. Berthollet tentang dua logam baru]. Annales de Chimie et de Physique. Seri ke-2 (dalam bahasa Prancis). 7: 199–206. Dari hlm. 203: "Cependant, pour rappeler les rapports de cette dernière avec le tellure, je l'ai nommée sélénium." (Namun, untuk mengingat kembali hubungan zat terakhir ini (selenium) dengan telurium, Saya menamainya "selenium".)
- ^ Weeks, Mary Elvira (1932). "The discovery of the elements. VI. Tellurium and selenium". Journal of Chemical Education. 9 (3): 474. Bibcode:1932JChEd...9..474W. doi:10.1021/ed009p474.
- ^ Trofast, Jan (2011). "Berzelius' Discovery of Selenium". Chemistry International. 33 (5): 16–19. PDF
- ^ Smith, Willoughby (1873). "The action of light on selenium". Journal of the Society of Telegraph Engineers. 2 (4): 31–33. doi:10.1049/jste-1.1873.0023.
- ^ Smith, Willoughby (20 Februari 1873). "Effect of light on selenium during the passage of an electric current". Nature. 7 (173): 303. Bibcode:1873Natur...7R.303.. doi:10.1038/007303e0
 .
.
- ^ Bonnier Corporation (1876). "Action of light on selenium". Popular Science. 10 (1): 116.
- ^ Levinshtein, M.E.; Simin, G.S. (1 Januari 1992). Earliest semiconductor device. Getting to Know Semiconductors. hlm. 77–79. ISBN 978-981-02-3516-1.
- ^ Winston, Brian (29 Mei 1998). Media Technology and Society: A History: From the Telegraph to the Internet. hlm. 89. ISBN 978-0-415-14229-8.
- ^ Morris, Peter Robin (1990). A History of the World Semiconductor Industry. hlm. 18. ISBN 978-0-86341-227-1.
- ^ Bergmann, Ludwig (1931). "Über eine neue Selen-Sperrschicht-Photozelle". Physikalische Zeitschrift. 32: 286–288.
- ^ Waitkins, G.R.; Bearse, A.E.; Shutt, R. (1942). "Industrial Utilization of Selenium and Tellurium". Industrial & Engineering Chemistry. 34 (8): 899–910. doi:10.1021/ie50392a002.
- ^ Pinsent, Jane (1954). "The need for selenite and molybdate in the formation of formic dehydrogenase by members of the Coli-aerogenes group of bacteria". Biochem. J. 57 (1): 10–16. doi:10.1042/bj0570010. PMC 1269698
 . PMID 13159942.
. PMID 13159942.
- ^ Stadtman, Thressa C. (2002). "Some Functions of the Essential Trace Element, Selenium". Trace Elements in Man and Animals 10. Trace Elements in Man and Animals. 10. hlm. 831–836. doi:10.1007/0-306-47466-2_267. ISBN 978-0-306-46378-5.
- ^ Schwarz, Klaus; Foltz, Calvin M. (1957). "Selenium as an Integral Part of Factor 3 Against Dietary Necrotic Liver Degeneration". Journal of the American Chemical Society. 79 (12): 3292–3293. doi:10.1021/ja01569a087.
- ^ Oldfield, James E. (2006). "Selenium: A historical perspective". Selenium. Selenium. hlm. 1–6. doi:10.1007/0-387-33827-6_1. ISBN 978-0-387-33826-2.
- ^ Hatfield, D. L.; Gladyshev, V.N. (2002). "How Selenium Has Altered Our Understanding of the Genetic Code". Molecular and Cellular Biology. 22 (11): 3565–3576. doi:10.1128/MCB.22.11.3565-3576.2002. PMC 133838
 . PMID 11997494.
. PMID 11997494.
- ^ "Native Selenium". Webminerals. Diakses tanggal 28 Juni 2023.
- ^ a b Kabata-Pendias, A. (1998). "Geochemistry of selenium". Journal of Environmental Pathology, Toxicology and Oncology. 17 (3–4): 173–177. PMID 9726787.
- ^ a b Fordyce, Fiona (2007). "Selenium Geochemistry and Health" (PDF). Ambio: A Journal of the Human Environment. 36 (1): 94–97. doi:10.1579/0044-7447(2007)36[94:SGAH]2.0.CO;2. PMID 17408199.
- ^ Wessjohann, Ludger A.; Schneider, Alex; Abbas, Muhammad; Brandt, Wolfgang (2007). "Selenium in chemistry and biochemistry in comparison to sulfur". Biological Chemistry. 388 (10): 997–1006. doi:10.1515/BC.2007.138. PMID 17937613.
- ^ Birringer, Marc; Pilawa, Sandra; Flohé, Leopold (2002). "Trends in selenium biochemistry". Natural Product Reports. 19 (6): 693–718. doi:10.1039/B205802M. PMID 12521265.
- ^ Amouroux, David; Liss, Peter S.; Tessier, Emmanuel; et al. (2001). "Role of oceans as biogenic sources of selenium". Earth and Planetary Science Letters. 189 (3–4): 277–283. Bibcode:2001E&PSL.189..277A. doi:10.1016/S0012-821X(01)00370-3.
- ^ Haug, Anna; Graham, Robin D.; Christophersen, Olav A.; Lyons, Graham H. (2007). "How to use the world's scarce selenium resources efficiently to increase the selenium concentration in food". Microbial Ecology in Health and Disease. 19 (4): 209–228. doi:10.1080/08910600701698986. PMC 2556185
 . PMID 18833333.
. PMID 18833333.
- ^ Rieuwerts, John (2015). The Elements of Environmental Pollution. London and New York: Earthscan Routledge. hlm. 262. ISBN 978-0-415-85919-6. OCLC 886492996.
- ^ "Public Health Statement: Selenium" (PDF). Agency for Toxic Substances and Disease Registry. Diakses tanggal 28 Juni 2023.
- ^ "Public Health Statement: Selenium – Production, Import/Export, Use, and Disposal" (PDF). Agency for Toxic Substances and Disease Registry. Diakses tanggal 28 Juni 2023.
- ^ "Chemistry: Periodic Table: selenium: key information". webelements. Diakses tanggal 28 Juni 2023.
- ^ Bartos, P.J. (2002). "SX-EW copper and the technology cycle". Resources Policy. 28 (3–4): 85–94. Bibcode:2002RePol..28...85B. doi:10.1016/S0301-4207(03)00025-4.
- ^ a b Naumov, A. V. (2010). "Selenium and tellurium: State of the markets, the crisis, and its consequences". Metallurgist. 54 (3–4): 197–200. doi:10.1007/s11015-010-9280-7.
- ^ Hoffmann, James E. (1989). "Recovering selenium and tellurium from copper refinery slimes". JOM. 41 (7): 33–38. Bibcode:1989JOM....41g..33H. doi:10.1007/BF03220269.
- ^ Hyvärinen, Olli; Lindroos, Leo; Yllö, Erkki (1989). "Recovering selenium from copper refinery slimes". JOM. 41 (7): 42–43. Bibcode:1989JOM....41g..42H. doi:10.1007/BF03220271.
- ^ a b c "Selenium and Tellurium: Statistics and Information". United States Geological Survey. Diakses tanggal 28 Juni 2023.
- ^ Feng, Renwei; Wei, Chaoyang; Tu, Shuxin (2013). "The roles of selenium in protecting plants against abiotic stresses". Environmental and Experimental Botany. 87: 58–68. doi:10.1016/j.envexpbot.2012.09.002.
- ^ Sun, Yan; Tian, Xike; He, Binbin; et al. (2011). "Studies of the reduction mechanism of selenium dioxide and its impact on the microstructure of manganese electrodeposit". Electrochimica Acta. 56 (24): 8305–8310. doi:10.1016/j.electacta.2011.06.111.
- ^ Bernd E. Langner "Selenium and Selenium Compounds" in Ullmann's Encyclopedia of Industrial Chemistry, 2005, Wiley-VCH, Weinheim. DOI:10.1002/14356007.a23_525.
- ^ Davis, Joseph R. (2001). Copper and Copper Alloys. ASM Int. hlm. 91. ISBN 978-0-87170-726-0.
- ^ Isakov, Edmund (2008-10-31). Cutting Data for Turning of Steel. hlm. 67. ISBN 978-0-8311-3314-6.
- ^ Gol'Dshtein, Ya. E.; Mushtakova, T. L.; Komissarova, T. A. (1979). "Effect of selenium on the structure and properties of structural steel". Metal Science and Heat Treatment. 21 (10): 741–746. Bibcode:1979MSHT...21..741G. doi:10.1007/BF00708374.
- ^ Davis, Joseph R. (2001). Copper and Copper Alloys. ASM International. hlm. 278. ISBN 978-0-87170-726-0.
- ^ Eftekhari, Ali (2017). "The rise of lithium–selenium batteries". Sustainable Energy & Fuels. 1: 14–29. doi:10.1039/C6SE00094K.
- ^ Deutsche Gesellschaft für Sonnenenergie (2008). "Copper indium diselenide (CIS) cell". Planning and Installing Photovoltaic Systems: A Guide for Installers, Architects and Engineers. Earthscan. hlm. 43–44. ISBN 978-1-84407-442-6.
- ^ Huang, Heyuan; Abbaszadeh, Shiva (2020). "Recent Developments of Amorphous Selenium-Based X-Ray Detectors: A Review". IEEE Sensors Journal. 20 (4): 1694–1704. Bibcode:2020ISenJ..20.1694H. doi:10.1109/JSEN.2019.2950319.
- ^ Kasap, Safa; Frey, Joel B.; Belev, George; Tousignant, Olivier; Mani, Habib; Laperriere, Luc; Reznik, Alla; Rowlands, John A. (2009). "Amorphous selenium and its alloys from early xeroradiography to high resolution X-ray image detectors and ultrasensitive imaging tubes". Physica Status Solidi (B). 246 (8): 1794–1805. Bibcode:2009PSSBR.246.1794K. doi:10.1002/pssb.200982007.
- ^ Springett, B. E. (1988). "Application of Selenium-Tellurium Photoconductors to the Xerographic Copying and Printing Processes". Phosphorus and Sulfur and the Related Elements. 38 (3–4): 341–350. doi:10.1080/03086648808079729.
- ^ Williams, Rob (2006). Computer Systems Architecture: A Networking Approach. Prentice Hall. hlm. 547–548. ISBN 978-0-321-34079-5.
- ^ Diels, Jean-Claude; Arissian, Ladan (2011). "The Laser Printer". Lasers. Wiley-VCH. hlm. 81–83. ISBN 978-3-527-64005-8.
- ^ Meller, Gregor; Grasser, Tibor (2009). Organic Electronics. Springer. hlm. 3–5. ISBN 978-3-642-04537-0.
- ^ Normile, Dennis (2000). "The birth of the Blues". Popular Science. hlm. 57.
- ^ Kasap, Safa; Frey, Joel B.; Belev, George; et al. (2009). "Amorphous selenium and its alloys from early xeroradiography to high resolution X-ray image detectors and ultrasensitive imaging tubes". Physica Status Solidi B. 246 (8): 1794–1805. Bibcode:2009PSSBR.246.1794K. doi:10.1002/pssb.200982007.
- ^ Svelto, Orazio (1998). Principles of LASERs fourth ed. Plenum. hlm. 457. ISBN 978-0-306-45748-7.
- ^ Singh, Fateh V.; Wirth, Thomas (2019). "Selenium reagents as catalysts". Catalysis Science & Technology. 9 (5): 1073–1091. doi:10.1039/C8CY02274G.
- ^ Hai-Fu, F.; Woolfson, M. M.; Jia-Xing, Y. (1993). "New Techniques of Applying Multi-Wavelength Anomalous Scattering Data". Proceedings of the Royal Society A: Mathematical, Physical and Engineering Sciences. 442 (1914): 13–32. Bibcode:1993RSPSA.442...13H. doi:10.1098/rspa.1993.0087.
- ^ MacLean, Marion E. (1937). "A project for general chemistry students: Color toning of photographic prints". Journal of Chemical Education. 14 (1): 31. Bibcode:1937JChEd..14...31M. doi:10.1021/ed014p31.
- ^ Penichon, Sylvie (1999). "Differences in Image Tonality Produced by Different Toning Protocols for Matte Collodion Photographs". Journal of the American Institute for Conservation. 38 (2): 124–143. doi:10.2307/3180042. JSTOR 3180042.
- ^ McKenzie, Joy (2003). Exploring Basic Black & White Photography
 . Delmar. hlm. 176. ISBN 978-1-4018-1556-1.
. Delmar. hlm. 176. ISBN 978-1-4018-1556-1.
- ^ Hayward, Peter; Currie, Dean. "Radiography of Welds Using Selenium 75, Ir 192 and X-rays" (PDF).
- ^ https://www.vichy.co.uk/on/demandware.static/-/Sites-vic-master-catalog/default/dw41dcc5e7/VIC/ProductImages/Blog-Imagery-Vichy/Vichy_Customer_Leaflet_Dandruff.pdf [URL PDF mentah]
- ^ Lemly, A. Dennis (1 September 2004). "Aquatic selenium pollution is a global environmental safety issue". Ecotoxicology and Environmental Safety (dalam bahasa Inggris). 59 (1): 44–56. doi:10.1016/S0147-6513(03)00095-2. ISSN 0147-6513. PMID 15261722.
- ^ Estruch, Ramon; Sacanella, Emilio; Ros, Emilio (4 Januari 2021). "Should we all go pesco-vegetarian?". European Heart Journal. 42 (12): 1144–1146. doi:10.1093/eurheartj/ehaa1088
 . ISSN 0195-668X. PMID 33393612 Periksa nilai
. ISSN 0195-668X. PMID 33393612 Periksa nilai |pmid=(bantuan). - ^ Gribble, Matthew; Karimi, Roxanne; Feingold, Beth; Nyland, Jennifer; O'Hara, Todd; Gladyshev, Michail; Chen, Celia (8 September 2015). "Mercury, selenium and fish oils in marine food webs and implications for human health". Journal of the Marine Biological Association of the United Kingdom. 1 (96): 43–59. doi:10.1017/S0025315415001356. PMC 4720108
 . PMID 26834292.
. PMID 26834292. at higher doses, selenium might be toxic to a range of animals including humans
- ^ Lemly, Dennis (1998). Selenium Assessment in Aquatic Ecosystems: A guide for hazard evaluation and water quality criteria. Springer. ISBN 0-387-95346-9.
- ^ Hamilton, Steven J. (29 Juni 2004). "Review of selenium toxicity in the aquatic food chain". Science of the Total Environment (dalam bahasa Inggris). 326 (1): 1–31. Bibcode:2004ScTEn.326....1H. doi:10.1016/j.scitotenv.2004.01.019. ISSN 0048-9697. PMID 15142762.
- ^ Lemly, D. (2004). "Aquatic selenium pollution is a global environmental safety issue". Ecotoxicology and Environmental Safety. 59 (1): 44–56. doi:10.1016/S0147-6513(03)00095-2. PMID 15261722.
- ^ Ohlendorf, H. M. (2003). Ecotoxicology of selenium. Handbook of ecotoxicology. Boca Raton: Lewis Publishers. hlm. 466–491. ISBN 978-1-56670-546-2.
- ^ Lemly, A. D. (1997). "A teratogenic deformity index for evaluating impacts of selenium on fish populations". Ecotoxicology and Environmental Safety. 37 (3): 259–266. doi:10.1006/eesa.1997.1554. PMID 9378093.
- ^ Penglase, S.; Hamre, K.; Ellingsen, S. (2014). "Selenium and mercury have a synergistic negative effect on fish reproduction". Aquatic Toxicology. 149: 16–24. doi:10.1016/j.aquatox.2014.01.020. PMID 24555955.
- ^ Heinz, G. H.; Hoffman, D. J. (1998). "Methylmercury chloride and selenomethionine interactions on health and reproduction in mallards". Environmental Toxicology and Chemistry. 17 (2): 139–145. doi:10.1002/etc.5620170202.
- ^ Atroshi, Faik (28 Mei 2014). Pharmacology and Nutritional Intervention in the Treatment of Disease (dalam bahasa Inggris). BoD – Books on Demand. ISBN 978-953-51-1383-6.
- ^ Freeman, John L.; Lindblom, Stormy Dawn; Quinn, Colin F.; Fakra, Sirine; Marcus, Matthew A.; Pilon-Smits, Elizabeth A. H. (2007). "Selenium accumulation protects plants from herbivory by Orthoptera via toxicity and deterrence". The New Phytologist. 175 (3): 490–500. doi:10.1111/j.1469-8137.2007.02119.x
 . ISSN 0028-646X. PMID 17635224.
. ISSN 0028-646X. PMID 17635224.
- ^ "Selenium concentrations in leaf material from Astragalus Oxyphysus (diablo locoweed) and Atriplex Lentiformis (quail bush) in the interior Coast Ranges and the western San Joaquin Valley, California". 1986.
- ^ Linus Pauling Institute at Oregon State University lpi.oregonstate.edu
- ^ Pakdel, Farzad; Ghazavi, Roghayeh; Heidary, Roghayeh; Nezamabadi, Athena; Parvizi, Maryam; Haji Safar Ali Memar, Mahsa; Gharebaghi, Reza; Heidary, Fatemeh (2019). "Effect of Selenium on Thyroid Disorders: Scientometric Analysis". Iranian Journal of Public Health. 48 (3): 410–420. ISSN 2251-6085. PMC 6570790
 . PMID 31223567.
. PMID 31223567.
- ^ "Selenium". Linus Pauling Institute di Oregon State University. Diakses tanggal 29 Juni 2023.
- ^ Mazokopakis, E. E.; Papadakis, J. A.; Papadomanolaki, M. G.; et al. (2007). "Effects of 12 months treatment with L-selenomethionine on serum anti-TPO Levels in Patients with Hashimoto's thyroiditis". Thyroid. 17 (7): 609–612. doi:10.1089/thy.2007.0040. PMID 17696828.
- ^ Ralston, N. V.; Ralston, C. R.; Blackwell, JL III; Raymond, L. J. (2008). "Dietary and tissue selenium in relation to methylmercury toxicity" (PDF). Neurotoxicology. 29 (5): 802–811. CiteSeerX 10.1.1.549.3878
 . doi:10.1016/j.neuro.2008.07.007. PMID 18761370. Diarsipkan dari versi asli (PDF) tanggal 24 Juli 2012. Diakses tanggal 29 Juni 2023.
. doi:10.1016/j.neuro.2008.07.007. PMID 18761370. Diarsipkan dari versi asli (PDF) tanggal 24 Juli 2012. Diakses tanggal 29 Juni 2023.
- ^ Penglase, S.; Hamre, K.; Ellingsen, S. (2014). "Selenium prevents downregulation of antioxidant selenoprotein genes by methylmercury". Free Radical Biology and Medicine. 75: 95–104. doi:10.1016/j.freeradbiomed.2014.07.019. hdl:1956/8708
 . PMID 25064324.
. PMID 25064324.
- ^ Usuki, F.; Yamashita, A.; Fujimura, M. (2011). "Post-transcriptional defects of antioxidant selenoenzymes cause oxidative stress under methylmercury exposure". The Journal of Biological Chemistry. 286 (8): 6641–6649. doi:10.1074/jbc.M110.168872
 . PMC 3057802
. PMC 3057802  . PMID 21106535.
. PMID 21106535.
- ^ Ohi, G.; Seki, H.; Maeda, H.; Yagyu, H. (1975). "Protective effect of selenite against methylmercury toxicity: observations concerning time, dose and route factors in the development of selenium attenuation". Industrial Health. 13 (3): 93–99. doi:10.2486/indhealth.13.93
 .
.
- ^ Ralston, NVC; Raymond, L. J. (2010). "Dietary selenium's protective effects against methylmercury toxicity". Toxicology. 278 (1): 112–123. doi:10.1016/j.tox.2010.06.004. PMID 20561558.
- ^ Carvalho, CML; Chew, Hashemy SI; Hashemy, J.; et al. (2008). "Inhibition of the human thioredoxin system: A molecular mechanism of mercury toxicity". Journal of Biological Chemistry. 283 (18): 11913–11923. doi:10.1074/jbc.M710133200
 . PMID 18321861.
. PMID 18321861.
- ^ Michiaki Yamashita, Shintaro Imamura, Md. Anwar Hossain, Ken Touhata, Takeshi Yabu, and Yumiko Yamashita, Strong antioxidant activity of the novel selenium-containing imidazole compound ″selenoneine″, The FASEB Journal, vol. 26 no. 1, supplement 969.13, April 2012
- ^ Yamashita, Y; Yabu, T; Yamashita, M (2010). "Discovery of the strong antioxidant selenoneine in tuna and selenium redox metabolism". World J Biol Chem. 1 (5): 144–50. doi:10.4331/wjbc.v1.i5.144. PMC 3083957
 . PMID 21540999.
. PMID 21540999.
- ^ Raymond, Laura; Ralston, Nicholas (November 2004). "Mercury: selenium interactions and health implications" (PDF). SMDJ Seychelles Medical and Dental Journal. 7: 72–77 – via Amalgam Information.
- ^ a b Gladyshev, Vadim N.; Hatfield, Dolph L. (1999). "Selenocysteine-containing proteins in mammals". Journal of Biomedical Science. 6 (3): 151–160. doi:10.1007/BF02255899. PMID 10343164.
- ^ Stadtman, T. C. (1996). "Selenocysteine". Annual Review of Biochemistry. 65 (1): 83–100. doi:10.1146/annurev.bi.65.070196.000503. PMID 8811175.
- ^ Lobanov, Alexey V.; Fomenko, Dmitri E.; Zhang, Yan; et al. (2007). "Evolutionary dynamics of eukaryotic selenoproteomes: large selenoproteomes may associate with aquatic life and small with terrestrial life". Genome Biology. 8 (9): R198. doi:10.1186/gb-2007-8-9-r198. PMC 2375036
 . PMID 17880704.
. PMID 17880704.
- ^ Venturi, Sebastiano; Venturi, Mattia (2007), "Evolution of Dietary Antioxidant Defences", European EpiMarker, 11 (3), hlm. 1–11
- ^ Castellano, Sergi; Novoselov, Sergey V.; Kryukov, Gregory V.; et al. (2004). "Reconsidering the evolution of eukaryotic selenoproteins: a novel nonmammalian family with scattered phylogenetic distribution". EMBO Reports. 5 (1): 71–7. doi:10.1038/sj.embor.7400036. PMC 1298953
 . PMID 14710190.
. PMID 14710190.
- ^ Kryukov, Gregory V.; Gladyshev, Vadim N. (2004). "The prokaryotic selenoproteome". EMBO Reports. 5 (5): 538–43. doi:10.1038/sj.embor.7400126. PMC 1299047
 . PMID 15105824.
. PMID 15105824.
- ^ Wilting, R.; Schorling, S.; Persson, B. C.; Böck, A. (1997). "Selenoprotein synthesis in archaea: identification of an mRNA element of Methanococcus jannaschii probably directing selenocysteine insertion". Journal of Molecular Biology. 266 (4): 637–41. doi:10.1006/jmbi.1996.0812. PMID 9102456.
- ^ Zhang, Yan; Fomenko, Dmitri E.; Gladyshev, Vadim N. (2005). "The microbial selenoproteome of the Sargasso Sea". Genome Biology. 6 (4): R37. doi:10.1186/gb-2005-6-4-r37. PMC 1088965
 . PMID 15833124.
. PMID 15833124.
- ^ Barclay, Margaret N. I.; MacPherson, Allan; Dixon, James (1995). "Selenium content of a range of UK food". Journal of Food Composition and Analysis. 8 (4): 307–318. doi:10.1006/jfca.1995.1025.
- ^ "Selenium Fact Sheet". ODS.OD.NIH.gov. US: The Office of Dietary Supplements, National Institutes of Health. (meliputi daftar makanan kaya selenium)
- ^ "FDA Issues Final Rule to Add Selenium to List of Required Nutrients for Infant Formula". www.fda.gov. Diarsipkan dari versi asli tanggal 14 November 2017. Diakses tanggal 29 Juni 2023.
- ^ A common reference for this is Schroeder, H. A.; Frost, D. V.; Balassa, J. J. (1970). "Essential trace metals in man: Selenium". Journal of Chronic Diseases. 23 (4): 227–43. doi:10.1016/0021-9681(70)90003-2. OSTI 6424964. PMID 4926392.
- ^ Zane Davis, T. (27 Maret 2008). "Selenium in Plants" (PDF). hlm. 8. Diakses tanggal 29 Juni 2023.
- ^ Baselt, R. (2008). Disposition of Toxic Drugs and Chemicals in Man (edisi ke-8). Foster City, CA: Biomedical Publications. hlm. 1416–1420. ISBN 978-0-9626523-5-6.
- ^ a b Razaghi, Ali; Poorebrahim, Mansour; Sarhan, Dhifaf; Björnstedt, Mikael (1 September 2021). "Selenium stimulates the antitumour immunity: Insights to future research". European Journal of Cancer (dalam bahasa English). 155: 256–267. doi:10.1016/j.ejca.2021.07.013
 . ISSN 0959-8049. PMID 34392068 Periksa nilai
. ISSN 0959-8049. PMID 34392068 Periksa nilai |pmid=(bantuan). - ^ "Dietary Supplement Fact Sheet: Selenium". National Institutes of Health; Office of Dietary Supplements. Diakses tanggal 29 Juni 2023.
- ^ Panel on Dietary Antioxidants and Related Compounds, Subcommittees on Upper Reference Levels of Nutrients and Interpretation and Uses of DRIs, Standing Committee on the Scientific Evaluation of Dietary Reference Intakes, Food and Nutrition Board, Institute of Medicine (15 Agustus 2000). Dietary Reference Intakes for Vitamin C, Vitamin E, Selenium, and Carotenoids. Institute of Medicine. hlm. 314–315. doi:10.17226/9810. ISBN 978-0-309-06949-6. PMID 25077263.
- ^ Yang, G.; Zhou, R. (1994). "Further Observations on the Human Maximum Safe Dietary Selenium Intake in a Seleniferous Area of China". Journal of Trace Elements and Electrolytes in Health and Disease. 8 (3–4): 159–165. PMID 7599506.
- ^ Yang, Guang-Qi; Xia, Yi-Ming (1995). "Studies on Human Dietary Requirements and Safe Range of Dietary Intakes of Selenium in China and Their Application in the Prevention of Related Endemic Diseases". Biomedical and Environmental Sciences. 8 (3): 187–201. PMID 8561918.
- ^ "Public Health Statement: Health Effects" (PDF). Agency for Toxic Substances and Disease Registry. Diakses tanggal 29 Juni 2023.
- ^ Wilber, C. G. (1980). "Toxicology of selenium". Clinical Toxicology. 17 (2): 171–230. doi:10.3109/15563658008985076. PMID 6998645.
- ^ Olson, O. E. (1986). "Selenium Toxicity in Animals with Emphasis on Man". International Journal of Toxicology. 5: 45–70. doi:10.3109/10915818609140736
 .
.
- ^ "Polo pony selenium levels up to 20 times higher than normal". 6 Mei 2009. Diarsipkan dari versi asli tanggal 2016-08-19. Diakses tanggal 29 Juni 2023.
- ^ a b Hamilton, Steven J.; Buhl, Kevin J.; Faerber, Neil L.; et al. (1990). "Toxicity of organic selenium in the diet to chinook salmon". Environ. Toxicol. Chem. 9 (3): 347–358. doi:10.1002/etc.5620090310.
- ^ a b Poston, H. A.; Combs, G. F. Jr.; Leibovitz, L. (1976). "Vitamin E and selenium interrelations in the diet of Atlantic salmon (Salmo salar): gross, histological and biochemical signs". Journal of Nutrition. 106 (7): 892–904. doi:10.1093/jn/106.7.892. PMID 932827.
- ^ Brain, P.; Cousens, R. (1989). "An equation to describe dose responses where there is stimulation of growth at low doses". Weed Research. 29 (2): 93–96. doi:10.1111/j.1365-3180.1989.tb00845.x.
- ^ "CDC – NIOSH Pocket Guide to Chemical Hazards – Selenium". www.cdc.gov. Diakses tanggal 29 Juni 2023.
- ^ Ravaglia, G.; Forti, P.; Maioli, F.; et al. (2000). "Effect of micronutrient status on natural killer cell immune function in healthy free-living subjects aged ≥90 y". American Journal of Clinical Nutrition. 71 (2): 590–598. doi:10.1093/ajcn/71.2.590
 . PMID 10648276.
. PMID 10648276.
- ^ MedSafe Editorial Team. "Selenium". Prescriber Update Articles. New Zealand Medicines and Medical Devices Safety Authority. Diakses tanggal 29 Juni 2023.
- ^ Ralston, N. V. C.; Raymond, L. J. (2010). "Dietary selenium's protective effects against methylmercury toxicity". Toxicology. 278 (1): 112–123. doi:10.1016/j.tox.2010.06.004. PMID 20561558.
- ^ Mann, Jim; Truswell, A. Stewart (2002). Essentials of Human Nutrition (edisi ke-2). Oxford University Press. ISBN 978-0-19-262756-8.
- ^ Moreno-Reyes, R.; Mathieu, F.; Boelaert, M.; et al. (2003). "Selenium and iodine supplementation of rural Tibetan children affected by Kashin-Beck osteoarthropathy". American Journal of Clinical Nutrition. 78 (1): 137–144. doi:10.1093/ajcn/78.1.137
 . PMID 12816783.
. PMID 12816783.
- ^ Kachuee, R.; Moeini, M.; Suori, M. (2013). "The effect of dietary organic and inorganic selenium supplementation on serum Se, Cu, Fe and Zn status during the late pregnancy in Merghoz goats and their kids". Small Ruminant Research. 110 (1): 20–27. doi:10.1016/j.smallrumres.2012.08.010.
- ^ National Research Council, Subcommittee on Sheep Nutrition (1985). Nutrient requirements of sheep. Edisi ke-6, National Academy Press, Washington, ISBN 0309035961.
- ^ a b National Research Council, Committee on Nutrient Requirements of Small Ruminants (2007). Nutrient requirements of small ruminants. National Academies Press, Washington, ISBN 0-309-10213-8.
- ^ Coop, I. E.; Blakely, R. L. (1949). "The metabolism and toxicity of cyanides and cyanogenic glycosides in sheep". N. Z. J. Sci. Technol. 30: 277–291.
- ^ Kraus, R. J.; Prohaska, J. R.; Ganther, H. E. (1980). "Oxidized forms of ovine erythrocyte glutathione peroxidase. Cyanide inhibition of 4-glutathione:4-selenoenzyme". Biochim. Biophys. Acta. 615 (1): 19–26. doi:10.1016/0005-2744(80)90004-2. PMID 7426660.
- ^ Kahn, C. M. (ed.) (2005). Merck veterinary manual. Edisi ke-9. Merck & Co., Inc., Whitehouse Station, ISBN 0911910506.
- ^ Rostami, Rahim; Nourooz-Zadeh, Sarmad; Mohammadi, Afshin; Khalkhali, Hamid Reza; Ferns, Gordon; Nourooz-Zadeh, Jaffar (31 Oktober 2020). "Serum Selenium Status and Its Interrelationship with Serum Biomarkers of Thyroid Function and Antioxidant Defense in Hashimoto's Thyroiditis". Antioxidants. 9 (11): E1070. doi:10.3390/antiox9111070
 . ISSN 2076-3921. PMC 7692168
. ISSN 2076-3921. PMC 7692168  . PMID 33142736 Periksa nilai
. PMID 33142736 Periksa nilai |pmid=(bantuan). - ^ Vanderpas, J. B.; Contempré, B.; Duale, N. L.; Deckx, H.; Bebe, N.; Longombé, A. O.; Thilly, C. H.; Diplock, A. T.; Dumont, J. E. (Februari 1993). "Selenium deficiency mitigates hypothyroxinemia in iodine-deficient subjects". The American Journal of Clinical Nutrition. 57 (2 Suppl): 271S–275S. doi:10.1093/ajcn/57.2.271S. ISSN 0002-9165. PMID 8427203.
Pranala luar
[sunting | sunting sumber]| Cari tahu mengenai Selenium pada proyek-proyek Wikimedia lainnya: | |
| Definisi dan terjemahan dari Wiktionary | |
| Gambar dan media dari Commons | |
| Buku dari Wikibuku | |
| Entri basisdata #Q876 di Wikidata | |
- (Inggris) Selenium di The Periodic Table of Videos (Universitas Nottingham)
- (Inggris) National Institutes of Health page on Selenium
- (Inggris) Assay Diarsipkan 26 Februari 2012 di Wayback Machine.
- (Inggris) ATSDR – Toxicological Profile: Selenium
- (Inggris) CDC – NIOSH Pocket Guide to Chemical Hazards
- (Inggris) Peter van der Krogt elements site
| (besar) | |||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | ||||||||||||||||
| 1 | H | He | |||||||||||||||||||||||||||||||
| 2 | Li | Be | B | C | N | O | F | Ne | |||||||||||||||||||||||||
| 3 | Na | Mg | Al | Si | P | S | Cl | Ar | |||||||||||||||||||||||||
| 4 | K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | |||||||||||||||
| 5 | Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | |||||||||||||||
| 6 | Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn | |
| 7 | Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |
|
| |||||||||||||||||||||||||||||||||










