Toremifen
| |
|---|---|
| |
| Nama sistematis (IUPAC) | |
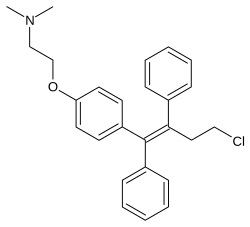
| 2-[4-[(1Z)-4-Kloro-1,2-difenil-but-1-en-1-il]fenoksi]-N,N-dimetiletanamina | |
| Data klinis | |
| Nama dagang | Fareston, dll |
| AHFS/Drugs.com | monograph |
| MedlinePlus | a608003 |
| Data lisensi | EMA:pranala |
| Kat. kehamilan | ? |
| Status hukum | ? |
| Rute | Oral |
| Data farmakokinetik | |
| Bioavailabilitas | Bagus/~100%[1][2] |
| Ikatan protein | 99.7%[1] |
| Metabolisme | Hati (CYP3A4)[3][2] |
| Waktu paruh | Toremifen: 3–7 hari[1] Metabolit: 4–21 hari[2][4][1] |
| Ekskresi | Feses: 70% (sebagai metabolit)[2] |
| Pengenal | |
| Nomor CAS | 89778-26-7 89778-27-8 (sitrat) |
| Kode ATC | L02BA02 |
| PubChem | CID 3005573 |
| Ligan IUPHAR | 4325 |
| DrugBank | DB00539 |
| ChemSpider | 2275722 |
| UNII | 7NFE54O27T |
| KEGG | D08620 |
| ChEBI | CHEBI:9635 |
| ChEMBL | CHEMBL1655 |
| Sinonim | (Z)-Toremifena; 4-Klorotamoksifen; 4-CT; Akapodena; CCRIS-8745; FC-1157; FC-1157a; GTx-006; NK-622; NSC-613680 |
| Data kimia | |
| Rumus | C26H28ClNO |
| |
Toremifen adalah obat yang digunakan dalam pengobatan kanker payudara stadium lanjut pada wanita pascamenopause.[4][5][6] Obat ini digunakan dengan cara diminum.[4]
Efek samping toremifen meliputi rasa panas, berkeringat, mual, muntah, pusing, keputihan, dan perdarahan vagina.[3][7] Obat ini juga dapat menyebabkan pembekuan darah, detak jantung tidak teratur, katarak, gangguan penglihatan, peningkatan enzim hati, hiperplasia endometrium, dan kanker endometrium. Kadar kalsium darah yang tinggi dapat terjadi pada wanita dengan metastasis tulang.[3]
Obat ini merupakan modulator reseptor estrogen selektif (SERM) dan karenanya merupakan agonis-antagonis reseptor campuran dari reseptor estrogen (ER), target biologis estrogen seperti estradiol.[3][7] Obat ini memiliki efek estrogenik pada tulang, hati, dan rahim serta efek antiestrogenik pada payudara.[5][8][9][3] Obat ini merupakan turunan trifeniletilena dan sangat mirip dengan tamoksifen.[10]
Toremifen diperkenalkan untuk penggunaan medis pada tahun 1997.[11][12] Obat ini merupakan antiestrogen pertama yang diperkenalkan sejak tamoksifen pada tahun 1978.[13] Obat ini tersedia sebagai obat generik.[14]
Sejarah
[sunting | sunting sumber]Toremifen diperkenalkan di Amerika Serikat pada tahun 1997.[11][12] Obat ini adalah antiestrogen pertama yang diperkenalkan di negara ini sejak tamoksifen pada tahun 1978.[13]
Kegunaan medis
[sunting | sunting sumber]Toremifen disetujui untuk pengobatan kanker payudara metastasis pada wanita pascamenopause dengan tumor reseptor estrogen positif atau tumor dengan status tidak diketahui.[4][5] Ini adalah satu-satunya penggunaan yang disetujui di Amerika Serikat.[4] Toremifen menunjukkan efektivitas yang setara dengan tamoksifen untuk indikasi ini.[5][15] Toremifen terbukti efektif dalam pengobatan nyeri payudara dan mungkin merupakan obat yang lebih efektif daripada tamoksifen untuk indikasi ini.[16] Toremifen juga memiliki efek yang lebih unggul pada kepadatan mineral tulang dan profil lipid, termasuk kadar kolesterol dan trigliserida, dibandingkan dengan tamoksifen.[15] Toremifen dilaporkan secara signifikan memperbaiki gejala ginekomastia pada pria.[17]
Bentuk yang tersedia
[sunting | sunting sumber]Toremifen tersedia dalam bentuk tablet oral 60 mg.[18][19]
Efek samping
[sunting | sunting sumber]Efek samping toremifen serupa dengan tamoksifen. Efek samping yang paling umum adalah hot flash. Efek samping lainnya termasuk berkeringat, mual, muntah, pusing, keputihan, dan perdarahan vagina. Pada wanita dengan metastasis tulang, hiperkalsemia dapat terjadi. Toremifen memiliki risiko kecil terjadinya kejadian tromboemboli. Katarak, gangguan penglihatan, dan peningkatan enzim hati telah dilaporkan.[3][7] Obat ini memperpanjang interval QT dan karenanya memiliki risiko disritmia yang berpotensi fatal. Risiko disritmia dapat dikurangi dengan menghindari penggunaan pada pasien dengan hipokalemia, hipomagnesemia, perpanjangan QT yang sudah ada sebelumnya, dan pada mereka yang mengonsumsi obat pemanjang QT lainnya. Karena toremifen memiliki aksi estrogenik di rahim, hal itu dapat meningkatkan risiko hiperplasia endometrium dan kanker endometrium.[3]
Toremifen tampaknya lebih aman daripada tamoksifen. Toremifen memiliki risiko lebih rendah terhadap tromboemboli vena (VTE) (misalnya, emboli paru), strok, dan katarak. Risiko VTE yang lebih rendah mungkin terkait dengan fakta bahwa tamoksifen menurunkan kadar anti-trombin III secara signifikan lebih besar daripada toremifen 60 atau 200 mg/hari.[15]
Interaksi
[sunting | sunting sumber]Toremifene adalah substrat CYP3A4, enzim sitokrom P450, dan karenanya obat yang menginduksi atau menghambat enzim ini masing-masing dapat menurunkan atau meningkatkan kadar toremifen dalam tubuh.[3]
Farmakologi
[sunting | sunting sumber]Farmakodinamik
[sunting | sunting sumber]Toremifen adalah modulator reseptor estrogen selektif (SERM).[3][7][20] Artinya, obat ini merupakan agonis–antagonis campuran selektif dari reseptor estrogen (ER), dengan aksi estrogenik pada beberapa jaringan dan aksi antiestrogenik pada jaringan lain.[3][7] Obat ini memiliki efek estrogenik pada tulang, efek estrogenik parsial pada rahim dan hati, serta efek antiestrogenik pada payudara.[5][8][9][3]
Afinitas toremifen untuk ER mirip dengan tamoksife.[5][21][22] Dalam penelitian menggunakan ER tikus, toremifen memiliki sekitar 1,4% dan tamoksifen memiliki sekitar 1,6% dari afinitas estradiol untuk ER.[23][24][25][26][27][22] Afinitas (Ki) toremifen pada ER manusia telah dilaporkan sebesar 20,3 ± 0,1 nM untuk ERα dan 15,4 ± 3,1 nM untuk ERβ.[20] Dalam studi ER tikus lainnya, toremifen memiliki 3–9% afinitas estradiol untuk ER; sementara metabolitnya N-desmetiltoremifen dan 4-hidroksitoremifen, memiliki 3–5% dan 64–158% afinitas estradiol untuk ER, masing-masing.[28][29][30] Afinitas metabolit lain, 4-hidroksi-N-desmetiltoremifen, tidak dinilai.[29] 4-Hidroksitoremifen menunjukkan potensi antiestrogenik sekitar 100 kali lipat lebih tinggi daripada toremifen in vitro dalam satu studi,[29] tetapi tidak dalam studi lain.[28] 4-Hidroksi-N-desmetiltoremifen juga ditemukan sangat antiestrogenik in vitro.[28] Metabolit toremifen, khususnya 4-hidroksitoremifen, dapat memberikan kontribusi penting terhadap aktivitas klinis obat tersebut.[1][29][28] Di sisi lain, beberapa otoritas menganggap toremifen bukan sebagai bakal obat.[31]
Toremifen sangat mirip dengan tamoksifen dan memiliki sebagian besar sifat yang sama.[5][8][9][3] Ada beberapa indikasi bahwa toremifen mungkin lebih aman daripada tamoksifen karena obat ini bukan hepatokarsinogen pada hewan dan mungkin memiliki potensi genotoksisitas yang lebih rendah. Namun, studi klinis tidak menemukan perbedaan signifikan antara toremifen dan tamoksifen, termasuk dalam hal efektivitas, tolerabilitas, dan keamanan; dan karenanya penggunaan klinis toremifen agak terbatas.[5][6] Toremifen diperkirakan memiliki sekitar sepertiga potensi tamoksifen; yaitu, 60 mg toremifen kira-kira setara dengan 20 mg tamoksifen dalam pengobatan kanker payudara.[32]
Toremifen telah ditemukan memiliki efek antigonadotropik pada wanita pascamenopause,[33] efek progonadotropik pada pria,[34] meningkatkan kadar globulin pengikat hormon seks,[33] dan menurunkan kadar faktor pertumbuhan mirip insulin 1 sekitar 20% pada wanita dan pria pascamenopause.[35]
Selain aktivitasnya sebagai SERM, 4-hidroksitoremifen merupakan antagonis reseptor terkait estrogen γ (ERRγ).[36]
Farmakokinetik
[sunting | sunting sumber]Absorpsi
[sunting | sunting sumber]Bioavailabilitas toremifen belum ditentukan secara tepat, tetapi diketahui baik dan diperkirakan sekitar 100%.[1][2] Kadar toremifen pada kondisi stabil dengan dosis 60 mg/hari adalah 800 hingga 879 ng/mL. Kadar N-desmetiltoremifen pada kondisi stabil dengan toremifen adalah 3.058 ng/mL pada 60 mg/hari, 5.942 ng/mL pada 200 mg/hari, dan 11.913 ng/mL pada 400 mg/hari. Kadar 4-hidroksitoremifen pada kondisi stabil dengan toremifen adalah 438 ng/mL pada 200 mg/hari, dan 889 ng/mL pada 400 mg/hari.[1] Konsentrasi toremifen meningkat secara linear pada rentang dosis 10 hingga 680 mg.[37][38]
Distribusi
[sunting | sunting sumber]Toremifen 99,7% terikat pada protein plasma, dengan 92% terikat secara spesifik pada albumin, sekitar 6% pada fraksi globulin β1, dan sekitar 2% pada fraksi antara albumin dan globulin α1.[37][1] Volume distribusi toremifen yang tampak berkisar antara 457 hingga 958 L.[37]
Metabolisme
[sunting | sunting sumber]Toremifen dimetabolisme di hati terutama oleh CYP3A4 dan kemudian mengalami hidroksilasi sekunder. Metabolit toremifen meliputi N-desmetiltoremifen, 4-hidroksitoremifen, dan 4-hidroksi-N-desmetiltoremifen, dan lain-lain.[1][29][2][39] Ospemifen (deaminohidroksitoremifen) juga merupakan metabolit utama toremifen.[1][4]
Eliminasi
[sunting | sunting sumber]Waktu paruh biologis toremifen adalah 3 hingga 7 hari pada individu yang sehat. Pada orang dengan gangguan fungsi hati, waktu paruhnya adalah 11 hari. Waktu paruh eliminasi metabolit toremifen adalah 5 hingga 21 hari untuk N-desmetiltoremifen, 5 hari untuk 4-hidroksitoremifen, dan 4 hari untuk ospemifen.[1][2][4] Waktu paruh eliminasi toremifen dan metabolitnya yang panjang diduga disebabkan oleh resirkulasi enterohepatik dan pengikatan protein plasma yang tinggi.[1][3] Toremifen dieliminasi 70% dalam feses sebagai metabolit.[2]
Kimia
[sunting | sunting sumber]Toremifen, juga dikenal sebagai 4-klorotamoksifen, merupakan turunan dari trifeniletilena dan analog dekat dari tamoksifen.[10] Ia juga berkerabat dekat dengan afimoksifen (4-hidroksitamoksifen) dan ospemifen (deaminohidroksitoremifen).[40][41]
Masyarakat dan budaya
[sunting | sunting sumber]Penelitian
[sunting | sunting sumber]Referensi
[sunting | sunting sumber]- ^ a b c d e f g h i j k l Taras TL, Wurz GT, Linares GR, DeGregorio MW (November 2000). "Clinical pharmacokinetics of toremifene". Clin Pharmacokinet. 39 (5): 327–34. doi:10.2165/00003088-200039050-00002. PMID 11108432.
- ^ a b c d e f g h DeVita Jr VT, Lawrence TS, Rosenberg SA (7 January 2015). DeVita, Hellman, and Rosenberg's Cancer: Principles & Practice of Oncology. Wolters Kluwer Health. hlm. 1126–. ISBN 978-1-4698-9455-3.
- ^ a b c d e f g h i j k l m Rosenthal L, Burchum J (17 February 2017). Lehne's Pharmacotherapeutics for Advanced Practice Providers - E-Book. Elsevier Health Sciences. hlm. 931–. ISBN 978-0-323-44779-9.
- ^ a b c d e f g "FARESTON (toremifene citrate) 60 mg Tablets oral administration" (PDF). GTx, Inc. U.S. Food and Drug Administration. March 2011.
- ^ a b c d e f g h Miller WR, Ingle JN (8 March 2002). Endocrine Therapy in Breast Cancer. CRC Press. hlm. 55–57. ISBN 978-0-203-90983-6.
- ^ a b Chabner BA, Longo DL (7 December 2011). Cancer Chemotherapy and Biotherapy: Principles and Practice. Lippincott Williams & Wilkins. hlm. 659–. ISBN 978-1-4511-4820-6.
- ^ a b c d e Schiff D, Arrillaga I, Wen PY (16 September 2017). Cancer Neurology in Clinical Practice: Neurological Complications of Cancer and its Treatment. Humana Press. hlm. 296–. ISBN 978-3-319-57901-6.
- ^ a b c Morrow M, Jordan VC (2003). Managing Breast Cancer Risk. PMPH-USA. hlm. 192–. ISBN 978-1-55009-260-8.
- ^ a b c Selective Estrogen Receptor Modulators—Advances in Research and Application: 2013 Edition: ScholarlyBrief. ScholarlyEditions. 1 May 2013. hlm. 51–. ISBN 978-1-4901-0447-8.
- ^ a b Cano A, Calaf i Alsina J, Duenas-Diez JL (22 September 2006). Selective Estrogen Receptor Modulators: A New Brand of Multitarget Drugs. Springer Science & Business Media. hlm. 52–. ISBN 978-3-540-34742-2.
- ^ a b Silva OE, Zurrida S (2005). Breast Cancer: A Practical Guide. Elsevier Health Sciences. hlm. 355–. ISBN 0-7020-2744-8.
- ^ a b Bidlack WR, Omaye ST, Meskin MS, Topham DK (16 March 2000). Phytochemicals as Bioactive Agents. CRC Press. hlm. 26–. ISBN 978-1-56676-788-0.
- ^ a b DiSaia PJ, Creasman WT, Mannel RS, McMeekin DS, Mutch DG (4 February 2017). Clinical Gynecologic Oncology E-Book. Elsevier Health Sciences. hlm. 124–. ISBN 978-0-323-44316-6.
- ^ "Generic Fareston Availability - Drugs.com". Drugs.com (dalam bahasa Inggris). Diakses tanggal 2019-04-19.
- ^ a b c Kesalahan pengutipan: Tag
<ref>tidak sah; tidak ditemukan teks untuk ref bernamapmid18062751 - ^ Bland KI, Copeland EM, Klimberg VS, Gradishar WJ (29 June 2017). The Breast E-Book: Comprehensive Management of Benign and Malignant Diseases. Elsevier Health Sciences. hlm. 86–. ISBN 978-0-323-51187-2.
- ^ Tabbal M, Fuleihan GE (2010). "Future Therapies". Osteoporosis in Men. hlm. 713–732. doi:10.1016/B978-0-12-374602-3.00057-2. ISBN 9780123746023.
- ^ Wirfs MJ (9 May 2019). The APRN and PA's Complete Guide to Prescribing Drug Therapy 2020. Springer Publishing Company. hlm. 60–. ISBN 978-0-8261-7934-0.
- ^ Casciato DA (2012). "Chapter 4: Cancer Chemotherapeutic Agents". Dalam Casciato DA, Territo MC. Manual of Clinical Oncology. Lippincott Williams & Wilkins. hlm. 122–. ISBN 978-1-4511-1560-4.
- ^ a b Taneja SS, Smith MR, Dalton JT, Raghow S, Barnette G, Steiner M, Veverka KA (March 2006). "Toremifene--a promising therapy for the prevention of prostate cancer and complications of androgen deprivation therapy". Expert Opin Investig Drugs. 15 (3): 293–305. doi:10.1517/13543784.15.3.293. PMID 16503765.
- ^ Workman P (6 December 2012). New Approaches in Cancer Pharmacology: Drug Design and Development. Springer Science & Business Media. hlm. 104–. ISBN 978-3-642-77874-2.
- ^ a b Kallio S, Kangas L, Blanco G, Johansson R, Karjalainen A, Perilä M, Pippo I, Sundquist H, Södervall M, Toivola R (1986). "A new triphenylethylene compound, Fc-1157a. I. Hormonal effects". Cancer Chemother Pharmacol. 17 (2): 103–8. doi:10.1007/BF00306736. PMID 2941176.
- ^ Wittliff JL, Kerr II JL, Andres SA (2005). "Estrogens IV: Estrogen-Like Pharmaceuticals". Dalam Wexler P. Encyclopedia of Toxicology, 2nd Edition. Dib-L. Elsevier. hlm. 254–258. ISBN 9780080548005.
- ^ Blair RM, Fang H, Branham WS, Hass BS, Dial SL, Moland CL, Tong W, Shi L, Perkins R, Sheehan DM (March 2000). "The estrogen receptor relative binding affinities of 188 natural and xenochemicals: structural diversity of ligands". Toxicol Sci. 54 (1): 138–53. doi:10.1093/toxsci/54.1.138
 . PMID 10746941.
. PMID 10746941.
- ^ Fang H, Tong W, Shi LM, Blair R, Perkins R, Branham W, Hass BS, Xie Q, Dial SL, Moland CL, Sheehan DM (March 2001). "Structure-activity relationships for a large diverse set of natural, synthetic, and environmental estrogens". Chem Res Toxicol. 14 (3): 280–94. doi:10.1021/tx000208y. PMID 11258977.
- ^ Chander SK, Sahota SS, Evans TR, Luqmani YA (December 1993). "The biological evaluation of novel antioestrogens for the treatment of breast cancer". Crit Rev Oncol Hematol. 15 (3): 243–69. doi:10.1016/1040-8428(93)90044-5. PMID 8142059.
- ^ Kavlock RJ, Daston GP (6 December 2012). Drug Toxicity in Embryonic Development II: Advances in Understanding Mechanisms of Birth Defects: Mechanistics Understanding of Human Development Toxicants. Springer Science & Business Media. hlm. 437–. ISBN 978-3-642-60447-8.
- ^ a b c d Kangas L (1990). "Biochemical and pharmacological effects of toremifene metabolites". Cancer Chemother Pharmacol. 27 (1): 8–12. doi:10.1007/BF00689269. PMID 2147128.
- ^ a b c d e Robinson SP, Parker CJ, Jordan VC (August 1990). "Preclinical studies with toremifene as an antitumor agent". Breast Cancer Res Treat. 16 (Suppl): S9–17. doi:10.1007/BF01807139. PMID 2149286.
- ^ Osborne CK (6 December 2012). Endocrine Therapies in Breast and Prostate Cancer. Springer Science & Business Media. hlm. 104–. ISBN 978-1-4613-1731-9.
- ^ Vogel CL, Johnston MA, Capers C, Braccia D (February 2014). "Toremifene for breast cancer: a review of 20 years of data". Clin Breast Cancer. 14 (1): 1–9. doi:10.1016/j.clbc.2013.10.014
 . PMID 24439786.
. PMID 24439786.
- ^ MacGregor JI, Jordan VC (June 1998). "Basic guide to the mechanisms of antiestrogen action". Pharmacol. Rev. 50 (2): 151–96. PMID 9647865.
- ^ a b Ellmén J, Hakulinen P, Partanen A, Hayes DF (November 2003). "Estrogenic effects of toremifene and tamoxifen in postmenopausal breast cancer patients" (PDF). Breast Cancer Res. Treat. 82 (2): 103–11. doi:10.1023/B:BREA.0000003957.54851.11. hdl:2027.42/44217
 . PMID 14692654.
. PMID 14692654.
- ^ Tsourdi E, Kourtis A, Farmakiotis D, Katsikis I, Salmas M, Panidis D (April 2009). "The effect of selective estrogen receptor modulator administration on the hypothalamic-pituitary-testicular axis in men with idiopathic oligozoospermia". Fertil. Steril. 91 (4 Suppl): 1427–30. doi:10.1016/j.fertnstert.2008.06.002
 . PMID 18692782.
. PMID 18692782.
- ^ Roelfsema F, Yang RJ, Takahashi PY, Erickson D, Bowers CY, Veldhuis JD (February 2018). "Effects of Toremifene, a Selective Estrogen Receptor Modulator, on Spontaneous and Stimulated GH Secretion, IGF-I, and IGF-Binding Proteins in Healthy Elderly Subjects". Journal of the Endocrine Society. 2 (2): 154–165. doi:10.1210/js.2017-00457. PMC 5789038
 . PMID 29383334.
. PMID 29383334.
- ^ Ariazi EA, Jordan VC (2006). "Estrogen-related receptors as emerging targets in cancer and metabolic disorders". Curr Top Med Chem. 6 (3): 203–15. doi:10.2174/1568026610606030203. PMID 16515477.
- ^ a b c Gennari L, Merlotti D, Stolakis K, Nuti R (April 2012). "Pharmacokinetic evaluation of toremifene and its clinical implications for the treatment of osteoporosis". Expert Opin Drug Metab Toxicol. 8 (4): 505–13. doi:10.1517/17425255.2012.665873. PMID 22356442.
- ^ Anttila M, Valavaara R, Kivinen S, Mäenpää J (June 1990). "Pharmacokinetics of toremifene". J Steroid Biochem. 36 (3): 249–52. doi:10.1016/0022-4731(90)90019-o. PMID 2142247.
- ^ Brenner GM, Stevens C (28 September 2017). Brenner and Stevens' Pharmacology E-Book. Elsevier Health Sciences. hlm. 394–. ISBN 978-0-323-39172-6.
- ^ Weber GF (22 July 2015). Molecular Therapies of Cancer. Springer. hlm. 304–. ISBN 978-3-319-13278-5.
- ^ Maximov PY, McDaniel RE, Jordan VC (23 July 2013). Tamoxifen: Pioneering Medicine in Breast Cancer. Springer Science & Business Media. hlm. 170–. ISBN 978-3-0348-0664-0.
Bacaan lebih lanjut
[sunting | sunting sumber]- Taras TL, Wurz GT, Linares GR, DeGregorio MW (2000). "Clinical pharmacokinetics of toremifene". Clin Pharmacokinet. 39 (5): 327–34. doi:10.2165/00003088-200039050-00002. PMID 11108432.
- Harvey HA, Kimura M, Hajba A (2006). "Toremifene: an evaluation of its safety profile". Breast. 15 (2): 142–57. doi:10.1016/j.breast.2005.09.007. PMID 16289904.
- Taneja SS, Smith MR, Dalton JT, Raghow S, Barnette G, Steiner M, Veverka KA (2006). "Toremifene--a promising therapy for the prevention of prostate cancer and complications of androgen deprivation therapy". Expert Opin Investig Drugs. 15 (3): 293–305. doi:10.1517/13543784.15.3.293. PMID 16503765.
- Zhou WB, Ding Q, Chen L, Liu XA, Wang S (2011). "Toremifene is an effective and safe alternative to tamoxifen in adjuvant endocrine therapy for breast cancer: results of four randomized trials". Breast Cancer Res. Treat. 128 (3): 625–31. doi:10.1007/s10549-011-1556-5. PMID 21553116.
- Gennari L, Merlotti D, Stolakis K, Nuti R (2012). "Pharmacokinetic evaluation of toremifene and its clinical implications for the treatment of osteoporosis". Expert Opin Drug Metab Toxicol. 8 (4): 505–13. doi:10.1517/17425255.2012.665873. PMID 22356442.
- Mao C, Yang ZY, He BF, Liu S, Zhou JH, Luo RC, Chen Q, Tang JL (2012). "Toremifene versus tamoxifen for advanced breast cancer". Cochrane Database Syst Rev. 2021 (7): CD008926. doi:10.1002/14651858.CD008926.pub2. PMC 8407374
 Periksa nilai
Periksa nilai |pmc=(bantuan). PMID 22786516. - Vogel CL, Johnston MA, Capers C, Braccia D (2014). "Toremifene for breast cancer: a review of 20 years of data". Clin. Breast Cancer. 14 (1): 1–9. doi:10.1016/j.clbc.2013.10.014
 . PMID 24439786.
. PMID 24439786. - Mustonen MV, Pyrhönen S, Kellokumpu-Lehtinen PL (2014). "Toremifene in the treatment of breast cancer". World J Clin Oncol. 5 (3): 393–405. doi:10.5306/wjco.v5.i3.393
 . PMC 4127610
. PMC 4127610  . PMID 25114854.
. PMID 25114854.
