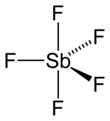
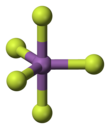
Antimon pentafluorida
Tampilan
| |||
| Nama | |||
|---|---|---|---|
| Nama IUPAC
antimon(V) fluorida
| |||
| Nama lain
Antimon pentafluorida
pentafluoridoantimon | |||
| Penanda | |||
Model 3D (JSmol)
|
|||
| 3DMet | {{{3DMet}}} | ||
| ChemSpider | |||
| Nomor EC | |||
PubChem CID
|
|||
| Nomor RTECS | {{{value}}} | ||
| Nomor UN | 1732 | ||
CompTox Dashboard (EPA)
|
|||
| |||
| |||
| Sifat | |||
| SbF5 | |||
| Massa molar | 216.74 g/mol | ||
| Penampilan | Cairan tidak berwarna higroskopik | ||
| Bau | Tajam | ||
| Densitas | 2.99 g/cm3[1] | ||
| Titik lebur | 83 °C (181 °F; 356 K) | ||
| Titik didih | 1.495 °C (2.723 °F; 1.768 K) | ||
| Bereaksi | |||
| Kelarutan | Dapat larut dalam KF, SO2 cair | ||
| Bahaya | |||
| Lembar data keselamatan | ICSC 0220 | ||
Klasifikasi UE (DSD) (usang)
|
Berbahaya (Xn) Berbahaya untuk lingkungan (N) | ||
| Frasa-R | R20/22, R51/53 | ||
| Frasa-S | S2, S61 | ||
| Batas imbas kesehatan AS (NIOSH): | |||
PEL (yang diperbolehkan)
|
TWA 0.5 mg/m3 (as Sb)[2] | ||
REL (yang direkomendasikan)
|
TWA 0.5 mg/m3 (as Sb)[2] | ||
| Senyawa terkait | |||
Anion lain
|
Antimon pentaklorida | ||
Kation lainnya
|
Fosfor pentafluorida Arsen pentafluorida Bismut pentafluorida | ||
Senyawa terkait
|
Antimon trifluorida | ||
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |||
| Referensi | |||
Antimon pentafluorida adalah senyawa anorganik dengan rumus SbF5. Senyawa cair tidak berwarna ini dapat dianggap sebagai asam Lewis dan merupakan komponen superasam asam fluoroantimonat, asam terkuat yang sejauh ini telah ditemukan. Senyawa ini dapat bereaksi dengan hampir semua senyawa yang ada.[3]
Pembuatan
[sunting | sunting sumber]Antimon pentafluorida dibuat dengan mereaksikan antimon pentaklorida dengan hidrogen fluorida anhidrat:[4]
- SbCl5 + 5 HF → SbF5 + 5 HCl
Senyawa ini juga dapat dibuat dari antimon trifluorida dan fluorin.[5]
Keamanan
[sunting | sunting sumber]SbF5 mengalami reaksi keras dengan berbagai macam senyawa dan sering kali mengeluarkan hidrogen fluorida yang berbahaya. Antimon pentafluorida sendiri bersifat korosif terhadap kulit dan mata.[6][7]
Referensi
[sunting | sunting sumber]- ^ Lide, David R., ed. (2006). CRC Handbook of Chemistry and Physics (edisi ke-87). Boca Raton, Florida: CRC Press. ISBN 0-8493-0487-3.
- ^ a b "NIOSH Pocket Guide to Chemical Hazards #0036". National Institute for Occupational Safety and Health (NIOSH).
- ^ Olah, G. A.; Prakash, G. K. S.; Wang, Q.; Li, X.-y."Antimony(V) Fluoride" in Encyclopedia of Reagents for Organic Synthesis (Ed: L. Paquette) 2004, J. Wiley & Sons, New York. DOI:10.1002/047084289.
- ^ Sabina C. Grund, Kunibert Hanusch, Hans J. Breunig, Hans Uwe Wolf "Antimony and Antimony Compounds" in Ullmann's Encyclopedia of Industrial Chemistry 2006, Wiley-VCH, Weinheim. DOI:10.1002/14356007.a03_055.pub2 10.1002/14356007.a03_055.pub2
- ^ Handbook of Preparative Inorganic Chemistry, 2nd Ed. Edited by G. Brauer, Academic Press, 1963, NY. Vol. 1. hlm. 200.
- ^ International Programme on Chemical Safety (2005). "Antimony pentafluoride". Commission of the European Communities (CEC). Diakses tanggal 2010-05-10.
- ^ Barbalace, Kenneth (2006). "Chemical Database - Antimony Pentafluoride". Environmental Chemistry. Diakses tanggal 2010-05-10.
Pranala luar
[sunting | sunting sumber]- WebBook page for SbF5
- National Pollutant Inventory - Antimony and compounds fact sheet
- National Pollutant Inventory - Fluoride compounds fact sheet